题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA |
| B、1mol H2O2完全分解生成H2O和O2时,转移了NA个电子 |
| C、1mol C10H22分子中,含有共价键数目为32NA |
| D、0.5mol Na2O2中含有NA个阴离子 |
考点:阿伏加德罗常数
专题:
分析:A、等物质的量铁和氯气反应生成氯化铁,铁过量,反应的电子转移根据氯气计算;
B、H2O2完全分解生成H2O和O2时,发生歧化反应;
C、依据烷烃的分子结构分析判断;
D、Na2O2由2个钠离子和1个过氧根构成.
B、H2O2完全分解生成H2O和O2时,发生歧化反应;
C、依据烷烃的分子结构分析判断;
D、Na2O2由2个钠离子和1个过氧根构成.
解答:
解:A、等物质的量铁和氯气反应生成氯化铁,铁过量,反应的电子转移根据氯气计算,转移电子数0.2NA,故A错误;
B、H2O2完全分解生成H2O和O2时,发生歧化反应,1mol H2O2转移1mol电子,故B正确;
C、C10H22符合烷烃通式,依据烷烃分子中的共价键都是单键,所以1molC10H22分子中,含有共价键数目=10-1+22=31mol,故C错误;
D、Na2O2由2个钠离子和1个过氧根构成,0.5mol Na2O2中含有0.5mol阴离子,个数为0.5NA个,故D错误.
故选B.
B、H2O2完全分解生成H2O和O2时,发生歧化反应,1mol H2O2转移1mol电子,故B正确;
C、C10H22符合烷烃通式,依据烷烃分子中的共价键都是单键,所以1molC10H22分子中,含有共价键数目=10-1+22=31mol,故C错误;
D、Na2O2由2个钠离子和1个过氧根构成,0.5mol Na2O2中含有0.5mol阴离子,个数为0.5NA个,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
某物质灼烧时,焰色反应为黄色,下列判断正确的是( )
| A、该物质一定是钠的化合物 |
| B、该物质一定含钠元素 |
| C、该物质一定是金属钠 |
| D、可确定该物质中不含钾元素 |
保护环境是公民的责任和义务.下列说法正确的是( )
| A、使用明矾净水的好处是杀菌、消毒,吸附水中的悬浮物 |
| B、减少使用氟氯代烃的目的是为了减少酸雨 |
| C、大量开采地下水,矿产资源,以满足社会经济发展的需求 |
| D、氢燃料汽车的使用,可以有效减少城市空气污染 |
有关下列说法正确的是( )
| A、6.8g熔融KHSO4与3.9g Na202阴离子数目相同 |
B、某金属阳离子的结构为: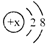 与Cl-形成的强电解质都是离子化合物 与Cl-形成的强电解质都是离子化合物 |
C、二硫化碳是直线型的分子,其电子式是: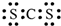 |
| D、因为氯、溴、碘非金属性逐渐减弱,所以其氢化物酸性HCl>HBr>HI |
下列有关物质的量的说法中,正确的是( )
| A、O3的摩尔质量为48g/mol |
| B、物质的量的单位是克 |
| C、1mol单质碳在任何条件下的体积都为22.4L |
| D、将2molNaCl晶体加入到1L水中,得到NaCl溶液的浓度就是2mol?L-1 |
下列物质均含有碳元素,其中属于氧化物的是( )
| A、C60 |
| B、CO |
| C、C2H2 |
| D、CH3OH |
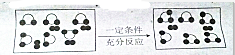 假设一定条件下某密闭容器中存在如图所示反应(空心球代表X原子,实心球代表Y原子),下列有关该反应的说法中不正确的是( )
假设一定条件下某密闭容器中存在如图所示反应(空心球代表X原子,实心球代表Y原子),下列有关该反应的说法中不正确的是( )| A、该反应一定是可逆反应 |
| B、该反应一定是氧化还原反应 |
| C、该反应一定是放热反应 |
| D、该反应的方程式可表示为2XY2+Y2?2XY3 |
 如图所示的装置,该装置中Cu极为
如图所示的装置,该装置中Cu极为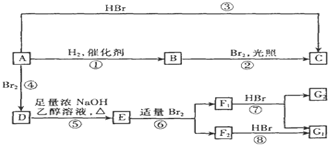 (D是
(D是 )
)