取100mL0.3mol/L的H2SO4溶液和300mL 0.25mol/L的H2SO4溶液注入500mL容量瓶中,再加水至刻度线,所得溶液中C(H2SO4)为.( )
| A、0.265mol/L |
| B、0.525mol/L |
| C、0.21mol/L |
| D、0.42mol/L |
有关化学用语不正确的是( )
| A、CO2分子的结构式:O=C=O | ||
B、O-18的原子符号:
| ||
C、S2-离子的结构示意图: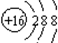 | ||
D、氯化氢分子的电子式: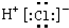 |
下列溶液中Cl-的物质的量浓度与l00mL1moL/LMgCl2溶液中Cl-的物质的量浓度相同的是( )
| A、50mL2mol/LCaCl2溶液 |
| B、100mL2moL/LNaCl溶液 |
| C、50mL4mol/LCaCl2溶液 |
| D、100mL4mol/LNaCl溶液 |
 下列关于1S电子在原子核外出现的概率分布图,也称电子云示意图(如图所示)的有关说法中,正确的是( )
下列关于1S电子在原子核外出现的概率分布图,也称电子云示意图(如图所示)的有关说法中,正确的是( )| A、通常用小黑点来表示电子的多少, |
| B、小黑点密度大,说明在该核外空间电子数目多 |
| C、通常用小黑点来表示电子绕核作高速圆周运动 |
| D、小黑点密,表示在该核外空间的单位体积内电子出现的机会大 |
下列离子中,电子数大于质子数且质子数大于中子数的是( )
| A、D3O+ |
| B、Li+ |
| C、OD- |
| D、OH- |
酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3+→Fe2+ Cl2→2Cl-HNO3→NO.MnO4-→
Mn2+ 分别用等物质的量的这些物质氧化足量的KI,得到I2最多 的是( )
Mn2+ 分别用等物质的量的这些物质氧化足量的KI,得到I2最多 的是( )
| A、Fe3+ |
| B、HNO3 |
| C、Cl2 |
| D、MnO4- |
已知下列热化学方程式:( )
(1)CH3COOH(1)+2O2(g)═2CO2(g)+2HO(1)△H1=-870.3kJ.mol-1
(2)C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
(3)H2(g)+
O2(g)═H2O(1)△H3=-285.8kJ.mol-1
则反应:2C(g)+2H2(g)+O2(g)═CH3COOH(1)的反应热为.
(1)CH3COOH(1)+2O2(g)═2CO2(g)+2HO(1)△H1=-870.3kJ.mol-1
(2)C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
(3)H2(g)+
| 1 |
| 2 |
则反应:2C(g)+2H2(g)+O2(g)═CH3COOH(1)的反应热为.
| A、-488.3kJ.mol-1 |
| B、-244.15kJ.mol-1 |
| C、+488.3kJ.mol-1 |
| D、+244.15-488.3kJ.mol-1 |
14 6 |
14 6 |
| A、质子数为14 |
| B、中子数为6 |
| C、电子数为6 |
| D、质量数为8 |
有关氧化还原反应的叙述正确的是( )
| A、氧化还原反应必然有氧元素的得失 |
| B、置换反应一定属于氧化还原反应 |
| C、某元素在化学反应中由化合态变为游离态,该元素可能被氧化,也可能被还原 |
| D、失电子越多还原性越强,得电子越多氧化性越强 |
 现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.
现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.