题目内容
取100mL0.3mol/L的H2SO4溶液和300mL 0.25mol/L的H2SO4溶液注入500mL容量瓶中,再加水至刻度线,所得溶液中C(H2SO4)为.( )
| A、0.265mol/L |
| B、0.525mol/L |
| C、0.21mol/L |
| D、0.42mol/L |
考点:物质的量浓度的相关计算
专题:
分析:混合后溶液中溶质硫酸的物质的量等于100mL 0.3mol?L-1和300mL 0.25mol?L-1的硫酸溶液中含有的硫酸之和,设混合后溶质硫酸的物质的量浓度为a,根据n=cV计算混合后的浓度.
解答:
解:混合后硫酸的物质的量不变,设混合后溶质硫酸的物质的量浓度为a,
则:0.1L×0.3mol?L-1+0.3L×0.25mol?L-1=0.5L×a,
解得:a=0.21mol/L,
故选C.
则:0.1L×0.3mol?L-1+0.3L×0.25mol?L-1=0.5L×a,
解得:a=0.21mol/L,
故选C.
点评:本题考查了物质的量浓度的计算,题目难度不大,试题侧重基础知识的考查,注意掌握物质的量浓度的概念及计算方法,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
下列各表述与示意图一致的是( )
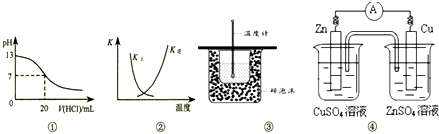

| A、图①表示25℃时,用0.1 mol?L-1盐酸滴定20 mL 0.1 mol?L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
| B、图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 |
| C、图③装置用于测定中和热 |
| D、图④装置可以构成锌、铜、硫酸铜溶液原电池 |
电子从4P能级跃迁到3d能级时,可通过光谱仪直接摄取( )
| A、原子的发射光谱 |
| B、原子的吸收光谱 |
| C、电子的运动轨迹图象 |
| D、电子体积大小的图象 |
下列离子中,电子数大于质子数且质子数大于中子数的是( )
| A、D3O+ |
| B、Li+ |
| C、OD- |
| D、OH- |
用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、22.4 L氢气中,一定含有氢原子2NA |
| B、在常温常压下,28gCO和N2的混合气体中含有的分子数为NA |
| C、常温下,pH=1的盐酸溶液,含有H+数目是0.1NA |
| D、标准状态下,2.7g铝和足量的浓硝酸反应,转移的电子数是0.3NA |
碳原子的摩尔质量是( )
| A、12 | B、12g/mol |
| C、12mol | D、12g |