题目内容
已知下列热化学方程式:( )
(1)CH3COOH(1)+2O2(g)═2CO2(g)+2HO(1)△H1=-870.3kJ.mol-1
(2)C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
(3)H2(g)+
O2(g)═H2O(1)△H3=-285.8kJ.mol-1
则反应:2C(g)+2H2(g)+O2(g)═CH3COOH(1)的反应热为.
(1)CH3COOH(1)+2O2(g)═2CO2(g)+2HO(1)△H1=-870.3kJ.mol-1
(2)C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
(3)H2(g)+
| 1 |
| 2 |
则反应:2C(g)+2H2(g)+O2(g)═CH3COOH(1)的反应热为.
| A、-488.3kJ.mol-1 |
| B、-244.15kJ.mol-1 |
| C、+488.3kJ.mol-1 |
| D、+244.15-488.3kJ.mol-1 |
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:由盖斯定律可知2×(2)+(3)×2-(1)得:2C(s)+2H2(g)+O2(g)=CH3COOH(l),则△H=2△H2+2△H3-△H1,带入数据进行计算.
解答:
解:已知(1)CH3COOH(1)+2O2(g)═2CO2(g)+2HO(1)△H1=-870.3kJ.mol-1
(2)C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
(3)H2(g)+
O2(g)═H2O(l)△H=-285.8kJ?mol-1
据盖斯定律,将方程式(2)×2+(3)×2-(1)得:
2C(s)+2H2(g)+O2(g)=CH3COOH(l),
则△H=2△H2+2△H3-△H1=2×(-393.5kJ?mol-1)+2×(-285.8kJ?mol-1)-(-870.3kJ.mol-1)=-488.3kJ.mol-1,
故选A.
(2)C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
(3)H2(g)+
| 1 |
| 2 |
据盖斯定律,将方程式(2)×2+(3)×2-(1)得:
2C(s)+2H2(g)+O2(g)=CH3COOH(l),
则△H=2△H2+2△H3-△H1=2×(-393.5kJ?mol-1)+2×(-285.8kJ?mol-1)-(-870.3kJ.mol-1)=-488.3kJ.mol-1,
故选A.
点评:本题考查化学反应与能量,侧重于盖斯定律的运用,注意把握盖斯定律的原理以及计算方法,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、凡是放热反应都是自发的,吸热反应都是非自发的 |
| B、自发反应一定是熵增大,非自发反应一定是熵减小 |
| C、熵增且放热的反应一定是自发反应 |
| D、非自发反应在任何条件下都不能实现 |
电子从4P能级跃迁到3d能级时,可通过光谱仪直接摄取( )
| A、原子的发射光谱 |
| B、原子的吸收光谱 |
| C、电子的运动轨迹图象 |
| D、电子体积大小的图象 |
下列溶液中Cl-的物质的量浓度与l00mL1moL/LMgCl2溶液中Cl-的物质的量浓度相同的是( )
| A、50mL2mol/LCaCl2溶液 |
| B、100mL2moL/LNaCl溶液 |
| C、50mL4mol/LCaCl2溶液 |
| D、100mL4mol/LNaCl溶液 |
用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、22.4 L氢气中,一定含有氢原子2NA |
| B、在常温常压下,28gCO和N2的混合气体中含有的分子数为NA |
| C、常温下,pH=1的盐酸溶液,含有H+数目是0.1NA |
| D、标准状态下,2.7g铝和足量的浓硝酸反应,转移的电子数是0.3NA |

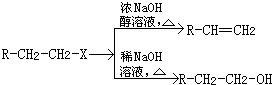
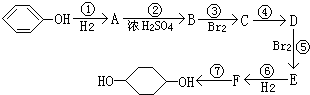
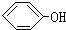 合成
合成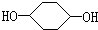 (部分试剂和反应条件已略去)
(部分试剂和反应条件已略去)