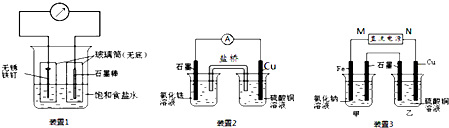
现有乙酸、环己烷、辛烯组成的混合物,其中氧的质量分数为a,则碳的质量分数是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
电子从4P能级跃迁到3d能级时,可通过光谱仪直接摄取( )
| A、原子的发射光谱 |
| B、原子的吸收光谱 |
| C、电子的运动轨迹图象 |
| D、电子体积大小的图象 |
下图各装置中,不能构成原电池的是( )
A、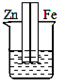 盐酸 |
B、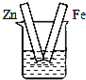 硫酸铜溶液 |
C、 稀硫酸 |
D、 稀硫酸 |
铅蓄电池在现代生活中有广泛的应用.其电极材料是Pb和PbO2,电解质是稀硫酸.Pb+PbO2+2H2SO4
2PbSO4+2H2O,下列说法正确的是( )
| 放电 |
| 充电 |
| A、铅蓄电池使用一段时间后要添加硫酸 |
| B、电池充电时,阴极反应为:Pb-2e-+SO42-═PbSO4 |
| C、电池充电时,电池正极应和电源的正极相连接 |
| D、电池放电时,电池正极周围溶液pH不断增大 |
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.下列有关该电池设计的说法不正确的是( )
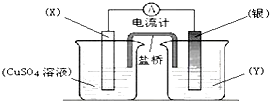

| A、电极X的材料是Cu |
| B、银电极为正极 |
| C、盐桥里Cl-移向电源的负极 |
| D、外电路中每通过0.2mol电子,银电极的质量理论上增加10.8g |
硫-碘循环分解水制氢主要涉及下列反应:
Ⅰ.SO2+2H2O+I2=H2SO4+2HI
Ⅱ.2HI?H2+I2
Ⅲ.2H2SO4=2SO2+O2+2H2O
分析上述反应,下列判断正确的是( )
Ⅰ.SO2+2H2O+I2=H2SO4+2HI
Ⅱ.2HI?H2+I2
Ⅲ.2H2SO4=2SO2+O2+2H2O
分析上述反应,下列判断正确的是( )
| A、循环过程中需补充H2O |
| B、反应I中SO2氧化性比HI强 |
| C、反应III易在常温下进行 |
| D、循环过程中产生1molO2的同时产生1 molH2 |
下列反应中,属于吸热反应的是( )
| A、乙醇燃烧 |
| B、Ba(OH)2?8H2O和NH4Cl固体反应 |
| C、铝与盐酸反应 |
| D、盐酸和氢氧化钠反应 |
如图所示的原电池,下列叙述正确的是(盐桥中装有含琼胶的KCl饱和溶液)( )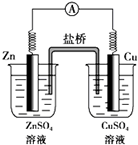

| A、反应中,盐桥中的Cl-会移向ZnSO4溶液 |
| B、取出盐桥后,电流计依然发生偏转 |
| C、铜片上有气泡逸出 |
| D、锌为负极,发生还原反应,电极反应式为:Zn-2e-=Zn2+ |