题目内容
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.下列有关该电池设计的说法不正确的是( )
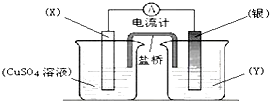

| A、电极X的材料是Cu |
| B、银电极为正极 |
| C、盐桥里Cl-移向电源的负极 |
| D、外电路中每通过0.2mol电子,银电极的质量理论上增加10.8g |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:由方程式2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)可知,反应中Ag+被还原,应为正极反应,则电解质溶液为硝酸银溶液,Cu被氧化,应为原电池负极反应,在装置图中X为Cu,Y为硝酸银溶液,以此解答该题.
解答:
解:A、Cu被氧化,应为原电池负极反应,在装置图中X为Cu,故A正确;
B、反应中Ag+被还原,应为正极反应,故B正确;
C、原电池中阴离子影响负极,故C正确;
D、外电路中每通过0.2mol电子,银电极的质量理论上增加2.16g,故D错误;
故选D.
B、反应中Ag+被还原,应为正极反应,故B正确;
C、原电池中阴离子影响负极,故C正确;
D、外电路中每通过0.2mol电子,银电极的质量理论上增加2.16g,故D错误;
故选D.
点评:本题考查原电池知识,为高考常见题型及高频考点,侧重于学生的分析能力和基本理论的理解和应用能力,难度不大,注意把握电极反应的判断和电极方程式的书写.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
常温下,设pH 均为5的H2SO4和A12(SO4)3溶液中由水电离出的c(H+)分别为c1、c2,则
是( )
| c1 |
| c2 |
| A、1 |
| B、104 |
| C、10-4 |
| D、10-14 |
下列说法中不正确的是( )
| A、蓄电池在放电过程中,负极质量增加,正极质量也增加 |
| B、电解法是最强有力的氧化还原手段,可以将极难还原的活泼金属从它们的化合物中还原出来 |
| C、钢铁发生吸氧腐蚀时,负极反应式为:Fe-3e-═Fe3+ |
| D、电解精炼铜时,用纯铜板作阴极,粗铜板作阳极,用硫酸铜溶液作电解液 |
某原电池工作时总的反应为Zn+Cu2+═Zn2++Cu,该原电池的组成可能是( )
| A、Zn为正极,Cu为负极,CuCl2溶液作电解质溶液 |
| B、Cu为正极,Zn为负极,稀H2SO4作电解质溶液 |
| C、Cu为正极,Zn为负极,CuSO4溶液作电解质溶液 |
| D、Fe为正极,Zn为负极,CuCl2溶液作电解质溶液 |
 下列关于1S电子在原子核外出现的概率分布图,也称电子云示意图(如图所示)的有关说法中,正确的是( )
下列关于1S电子在原子核外出现的概率分布图,也称电子云示意图(如图所示)的有关说法中,正确的是( )| A、通常用小黑点来表示电子的多少, |
| B、小黑点密度大,说明在该核外空间电子数目多 |
| C、通常用小黑点来表示电子绕核作高速圆周运动 |
| D、小黑点密,表示在该核外空间的单位体积内电子出现的机会大 |
下列离子方程式中,正确的是( )
| A、氧化亚铁与稀盐酸反应:FeO+2H+=Fe3++H2O |
| B、向氯化铜溶液中加入氢氧化钠溶液:Cu2++OH-=Cu(OH)2↓ |
| C、氯化铁溶液与铜反应:Fe3++Cu=Cu2++Fe2+ |
| D、向氯化亚铁溶液中通入氯气:2Fe2++Cl2=2Fe3++2Cl- |