题目内容
下图各装置中,不能构成原电池的是( )
A、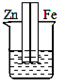 盐酸 |
B、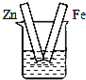 硫酸铜溶液 |
C、 稀硫酸 |
D、 稀硫酸 |
考点:原电池和电解池的工作原理
专题:
分析:原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,据此分析解答.
解答:
解:A.该装置符合原电池的构成条件,属于原电池,Zn易失电子作负极,Fe作正极,故A不选;
B.该装置符合原电池的构成条件,属于原电池,Zn易失电子作负极,Fe作正极,故B不选;
C.该装置符合原电池的构成条件,属于原电池,Fe易失电子作负极,C作正极,故C不选;
D.该装置没有形成闭合回路,所以不能构成原电池,故D选;
故选D.
B.该装置符合原电池的构成条件,属于原电池,Zn易失电子作负极,Fe作正极,故B不选;
C.该装置符合原电池的构成条件,属于原电池,Fe易失电子作负极,C作正极,故C不选;
D.该装置没有形成闭合回路,所以不能构成原电池,故D选;
故选D.
点评:本题考查了原电池的判断,根据原电池的构成条件来分析解答,这几个条件必须同时具备才能构成原电池,缺一不可,题目难度不大.

练习册系列答案
相关题目
在由水电离出的C[OH-]=1×10-13mol/L的溶液中,能大量共存的离子组是( )
| A、Fe2+ Na+ NO3- Cl- |
| B、Ba2+ Na+ NO3- Cl- |
| C、SO42- SO32- NH4+ Na+ |
| D、Mg2+ Na+ Br- ClO- |
铝片与盐酸的反应属于( )
| A、吸热反应 |
| B、放热反应 |
| C、氧化还原反应 |
| D、非氧化还原反应 |
如图所示的原电池,下列叙述正确的是(盐桥中装有含琼胶的KCl饱和溶液)( )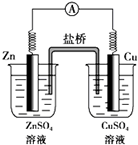

| A、反应中,盐桥中的Cl-会移向ZnSO4溶液 |
| B、取出盐桥后,电流计依然发生偏转 |
| C、铜片上有气泡逸出 |
| D、锌为负极,发生还原反应,电极反应式为:Zn-2e-=Zn2+ |
14 6 |
14 6 |
| A、质子数为14 |
| B、中子数为6 |
| C、电子数为6 |
| D、质量数为8 |
有关化学用语不正确的是( )
| A、CO2分子的结构式:O=C=O | ||
B、O-18的原子符号:
| ||
C、S2-离子的结构示意图: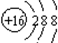 | ||
D、氯化氢分子的电子式: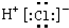 |
下列方程式书写不正确的是( )
| A、NaHS水解:HS-+H2O?H2S+OH- |
| B、氢氧化钡溶于水电离:Ba(OH)2═Ba2++2OH- |
| C、醋酸溶于水电离:CH3COOH?CH3COO-+H+ |
| D、碳酸钠水解:CO32-+2H2O?2OH-+H2CO3 |