0 129320 129328 129334 129338 129344 129346 129350 129356 129358 129364 129370 129374 129376 129380 129386 129388 129394 129398 129400 129404 129406 129410 129412 129414 129415 129416 129418 129419 129420 129422 129424 129428 129430 129434 129436 129440 129446 129448 129454 129458 129460 129464 129470 129476 129478 129484 129488 129490 129496 129500 129506 129514 203614
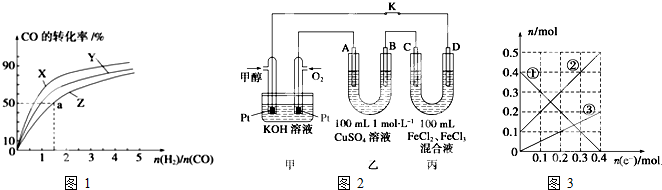
 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(如图中的△H表示生成lmol产物的数据).
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(如图中的△H表示生成lmol产物的数据).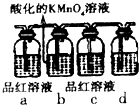 掌握物质之间的转化,是学习元素化合物知识的基础.
掌握物质之间的转化,是学习元素化合物知识的基础.
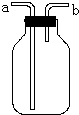 (1)如图的装置在实验室中用途比较广泛:
(1)如图的装置在实验室中用途比较广泛: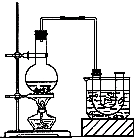 已知:CH3CH2OH+NaBr+H2SO4(浓)
已知:CH3CH2OH+NaBr+H2SO4(浓) 用实验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸,其具体实验步骤如下:
用实验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸,其具体实验步骤如下: 下表是元素周期表一部分,表中所列字母分别代表某一化学元素.
下表是元素周期表一部分,表中所列字母分别代表某一化学元素.