题目内容
 用实验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸,其具体实验步骤如下:
用实验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸,其具体实验步骤如下:①取一支碱式滴定管(如图中有两只滴定管,你选择哪一只?)
②用酸式滴定管精确地放出25.00mL待测盐酸,置于用蒸馏水洗净的锥形瓶中.再加入酚酞试液2滴;
③滴定时,边滴边振荡,同时眼睛注视锥形瓶内溶液颜色的变化,当锥形瓶内溶液由
④记录液面刻度读数.根据滴定管的两次读数得出消耗标准NaOH的体积,再重复测定两次,实验结果记录见下表:
| 实验次数 | 起始滴定管读数 | 终点滴定管读数 |
| 1 | 0.00mL | 24.02mL |
| 2 | 0.50mL | 24.46mL |
| 3 | 1.00mL | 25.02mL |
⑤如果滴定结束时俯视碱式滴定管刻度读数(其它操作均正确),则对滴定结果稀盐酸浓度的影响是
考点:中和滴定
专题:实验题
分析:①根据碱式滴定管下端为橡皮管;
③选择酚酞,观察到锥形瓶中溶液的颜色由无色变为浅红色,且半分钟不褪色,则达到滴定终点;
④先根据数据的有效性,舍去第3组数据,然后求出1、2组平均消耗V(NaOH),接着根据c(待测)=
计算;
⑤根据c(待测)=
分析不当操作对V(标准)的影响,以此判断;
③选择酚酞,观察到锥形瓶中溶液的颜色由无色变为浅红色,且半分钟不褪色,则达到滴定终点;
④先根据数据的有效性,舍去第3组数据,然后求出1、2组平均消耗V(NaOH),接着根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
⑤根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
解答:
解:①碱式滴定管下端为橡皮管,所以碱式滴定管b;
故答案为:b;
③选择酚酞,观察到锥形瓶中溶液的颜色由无色变为浅红色,且半分钟不褪色,则达到滴定终点;
故答案为:由无色变为浅红色;
④三次滴定消耗的体积为:24.02mL,23.96mL,24.02mL,均有效,三组平均消耗V(NaOH)=24.00mL,c(待测)=
=
=0.096mol/L;
故答案为:0.096mol/L;
⑤A.滴定终点读数时,俯视滴定管的刻度,导致氢氧化钠溶液体积偏小,所以所测盐酸浓度偏小,故错误;
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗,待测液的物质的量不变,所用氢氧化钠溶液体积不变,所测盐酸浓度不变,故B错误;
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液,所用氢氧化钠溶液体积偏大,所测盐酸浓度偏大,故C正确;
D.未用标准液润洗碱式滴定管,氢氧化钠溶液浓度偏小,所用氢氧化钠溶液体积偏大,所测盐酸浓度偏大,故D正确;
E.滴定前锥形瓶用蒸馏水洗净后未干燥,待测液的物质的量不变,所用氢氧化钠溶液体积不变,所测盐酸浓度不变,故E错误;
故选:CD;
⑤滴定终点读数时,俯视滴定管的刻度,导致氢氧化钠溶液体积偏小,根据c(待测)=
分析,所测盐酸浓度偏小;
故答案为:偏低;
故答案为:b;
③选择酚酞,观察到锥形瓶中溶液的颜色由无色变为浅红色,且半分钟不褪色,则达到滴定终点;
故答案为:由无色变为浅红色;
④三次滴定消耗的体积为:24.02mL,23.96mL,24.02mL,均有效,三组平均消耗V(NaOH)=24.00mL,c(待测)=
| V(标准)×c(标准) |
| V(待测) |
| 0.100mol/L×24.00mL |
| 25.00mL |
故答案为:0.096mol/L;
⑤A.滴定终点读数时,俯视滴定管的刻度,导致氢氧化钠溶液体积偏小,所以所测盐酸浓度偏小,故错误;
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗,待测液的物质的量不变,所用氢氧化钠溶液体积不变,所测盐酸浓度不变,故B错误;
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液,所用氢氧化钠溶液体积偏大,所测盐酸浓度偏大,故C正确;
D.未用标准液润洗碱式滴定管,氢氧化钠溶液浓度偏小,所用氢氧化钠溶液体积偏大,所测盐酸浓度偏大,故D正确;
E.滴定前锥形瓶用蒸馏水洗净后未干燥,待测液的物质的量不变,所用氢氧化钠溶液体积不变,所测盐酸浓度不变,故E错误;
故选:CD;
⑤滴定终点读数时,俯视滴定管的刻度,导致氢氧化钠溶液体积偏小,根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
故答案为:偏低;
点评:本题主要考查酸碱中和滴定,明确实验的原理、注意事项、数据处理等即可解答,题目难度中等.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
已知强酸与强碱的稀溶液发生中和反应的热化学方程式为:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1,又知电解质的电离是吸热过程.向1L 0.5mol?L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓硫酸;③稀硝酸,恰好完全反应.其焓变△H1、△H2、△H3的关系是( )
| A、△H1>△H2>△H3 |
| B、△H1<△H3<△H2 |
| C、△H1=△H3>△H2 |
| D、△H1>△H3>△H2 |
某有机物甲经氧化后得乙(分子式为C2H3O2Cl);而甲经水解可得丙,1mol丙和2mol乙反应的一种含氯的酯(C6H8O4Cl2).由此推断甲的结构简式为( )
| A、HO-CH2-CH2-OH |
B、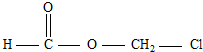 |
C、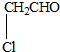 |
D、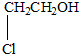 |
对于某些离子的检验及结论一定正确的是( )
| A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32? |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42? |
| C、加入氯水后再加入KSCN溶液,溶液变红色,一定有Fe2+ |
| D、加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
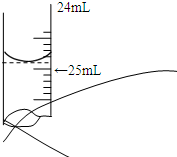 欲测定某NaOH溶液的物质的量浓度,可用0.1000mol?L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂).请回答下列问题:
欲测定某NaOH溶液的物质的量浓度,可用0.1000mol?L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂).请回答下列问题: