题目内容
某化学课外小组同学在实验室做酸碱中和滴定实验,他们准确移取25.00ml某未知浓度的盐酸溶液于一洁净锥形瓶中,然后用0.2000mol/LNaOH溶液滴定(指示剂为酚酞).滴定结果如下:
(1)根据以上数据可计算出盐酸的物质的量浓度为 mol/L.(精确到0.0001)
(2)下列有关滴定的操作正确的顺序是
①用标准液润洗滴定管
②往滴定管中注入标准溶液
③检查滴定管是否漏水
④滴定
⑤加水洗涤
A.⑤①③②④B.③⑤①②④C.⑤②③①④D.②①③⑤④
(3)若操作有误,则导致待测盐酸溶液浓度偏低的错误操作是
A.滴定管用蒸馏水洗后未用标准碱液润洗,直接装入标准碱液
B.滴定前滴定管尖端有气泡,滴后气泡消失
C.滴定管读数时,滴定前仰视滴定后俯视
D.待测液中指示剂酚酞(为有机弱酸)加得太多
(4)如果准确移取25.00mL 0.2000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度? 填“是”或“否”)
(5)另一小组同学用标准盐酸滴定未知浓度的NaOH溶液,若测定结果偏高,则产生误差的原因可能是
A.滴定时,装NaOH溶液的锥形瓶未用NaOH溶液润洗
B.酸式滴定管用蒸馏水洗后,未用标准盐酸润洗
C.滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失
D.配置NaOH溶液时,NaOH固体中混有少量KOH固体.
| NaOH溶液起始读数 | NaOH溶液终点读数 | |
| 第一次 | 0.02mL | 18.60mL |
| 第二次 | 0.04mL | 18.66mL |
| 第三次 | 0.20mL | 20.60mL |
(2)下列有关滴定的操作正确的顺序是
①用标准液润洗滴定管
②往滴定管中注入标准溶液
③检查滴定管是否漏水
④滴定
⑤加水洗涤
A.⑤①③②④B.③⑤①②④C.⑤②③①④D.②①③⑤④
(3)若操作有误,则导致待测盐酸溶液浓度偏低的错误操作是
A.滴定管用蒸馏水洗后未用标准碱液润洗,直接装入标准碱液
B.滴定前滴定管尖端有气泡,滴后气泡消失
C.滴定管读数时,滴定前仰视滴定后俯视
D.待测液中指示剂酚酞(为有机弱酸)加得太多
(4)如果准确移取25.00mL 0.2000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?
(5)另一小组同学用标准盐酸滴定未知浓度的NaOH溶液,若测定结果偏高,则产生误差的原因可能是
A.滴定时,装NaOH溶液的锥形瓶未用NaOH溶液润洗
B.酸式滴定管用蒸馏水洗后,未用标准盐酸润洗
C.滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失
D.配置NaOH溶液时,NaOH固体中混有少量KOH固体.
考点:中和滴定
专题:
分析:(1)先判断数据的合理性,然后NaOH溶液的平均体积,然后根据HCl~NaOH求盐酸的物质的量浓度;
(2)中和滴定按照检漏、洗涤、润洗、装液、取待测液、滴定等顺序操作;
(3)根据c(待)=
分析不当操作对V(标)的影响,以此判断浓度的误差;
(4)根据关系式HCl~NaOH来计算出盐酸的浓度;
(5)根据c(待)=
分析不当操作对V(标)的影响,以此判断浓度的误差.
(2)中和滴定按照检漏、洗涤、润洗、装液、取待测液、滴定等顺序操作;
(3)根据c(待)=
| c(标)×V(标) |
| V(待) |
(4)根据关系式HCl~NaOH来计算出盐酸的浓度;
(5)根据c(待)=
| c(标)×V(标) |
| V(待) |
解答:
解:(1)三次消耗的NaOH溶液的体积分别为:18.58mL,18.62mL,20.40mL,第3组数据相差较大,舍去,其他两次消耗盐酸溶液的平均体积为18.60mL;
HCl~NaOH
1 1
c(HCl)×25.00mL 0.20mol/L×18.60mL
解得:c(HCl)=0.1488mol/L,
故答案为:0.1488;
(2)中和滴定按照检漏、洗涤、润洗、装液、取待测液、滴定等顺序操作,所以滴定的操作正确的顺序是③⑤①②④,故选B.
(3)A.滴定管用蒸馏水洗后未用标准碱液润洗,直接装入标准碱液,标准液浓度减小,造成V(标)偏大,根据c(待)=
分析,可知c(待)偏大,故A错误;
B.滴定前滴定管尖端有气泡,滴后气泡消失,造成V(标)偏大,根据c(待)=
分析,可知c(待)偏大,故B错误;
C.滴定管读数时,滴定前仰视滴定后俯视,造成V(标)偏小,根据c(待)=
分析,可知c(待)偏小,故C正确;
D.待测液中指示剂酚酞(为有机弱酸)加得太多,消耗的碱偏多,造成V(标)偏大,根据c(待)=
分析,可知c(待)偏大,故D错误;
故选C;
(4)准确移取20.00mL 0.1000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,通过盐酸的体积,根据HCl~NaOH来计算出盐酸的浓度,故答案为:是;
(5)A.滴定时,装NaOH溶液的锥形瓶未用NaOH溶液润洗,氢氧化钠溶液被稀释,造成V(标)偏小,根据c(待)=
分析,可知c(待)偏小,故A错误;
B.酸式滴定管用蒸馏水洗后,未用标准盐酸润洗,标准盐酸被稀释,造成V(标)偏大,根据c(待)=
分析,可知c(待)偏大,故B正确;
C.滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失,造成V(标)偏大,根据c(待)=
分析,可知c(待)偏大,故C正确;
D.相同质量的氢氧化钠和氢氧化钾,氢氧化钠的物质的量大于氢氧化钾的物质的量,所以配置NaOH溶液时,NaOH固体中混有少量KOH固体,造成V(标)偏小,根据c(待)=
分析,可知c(待)偏小,故D错误;
故选BC.
HCl~NaOH
1 1
c(HCl)×25.00mL 0.20mol/L×18.60mL
解得:c(HCl)=0.1488mol/L,
故答案为:0.1488;
(2)中和滴定按照检漏、洗涤、润洗、装液、取待测液、滴定等顺序操作,所以滴定的操作正确的顺序是③⑤①②④,故选B.
(3)A.滴定管用蒸馏水洗后未用标准碱液润洗,直接装入标准碱液,标准液浓度减小,造成V(标)偏大,根据c(待)=
| c(标)×V(标) |
| V(待) |
B.滴定前滴定管尖端有气泡,滴后气泡消失,造成V(标)偏大,根据c(待)=
| c(标)×V(标) |
| V(待) |
C.滴定管读数时,滴定前仰视滴定后俯视,造成V(标)偏小,根据c(待)=
| c(标)×V(标) |
| V(待) |
D.待测液中指示剂酚酞(为有机弱酸)加得太多,消耗的碱偏多,造成V(标)偏大,根据c(待)=
| c(标)×V(标) |
| V(待) |
故选C;
(4)准确移取20.00mL 0.1000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,通过盐酸的体积,根据HCl~NaOH来计算出盐酸的浓度,故答案为:是;
(5)A.滴定时,装NaOH溶液的锥形瓶未用NaOH溶液润洗,氢氧化钠溶液被稀释,造成V(标)偏小,根据c(待)=
| c(标)×V(标) |
| V(待) |
B.酸式滴定管用蒸馏水洗后,未用标准盐酸润洗,标准盐酸被稀释,造成V(标)偏大,根据c(待)=
| c(标)×V(标) |
| V(待) |
C.滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失,造成V(标)偏大,根据c(待)=
| c(标)×V(标) |
| V(待) |
D.相同质量的氢氧化钠和氢氧化钾,氢氧化钠的物质的量大于氢氧化钾的物质的量,所以配置NaOH溶液时,NaOH固体中混有少量KOH固体,造成V(标)偏小,根据c(待)=
| c(标)×V(标) |
| V(待) |
故选BC.
点评:本题考查酸碱中和滴定实验,难度不大,注意把握实验的原理、步骤、方法以及注意事项,把握实验基本操作.

练习册系列答案
相关题目
与6.4g SO2所含的氧原子数相等的NO2的质量是( )
| A、3.2g | B、4.6g |
| C、6.4g | D、2.3g |
己烯雌酚是一种激素类药物,结构如下.下列有关叙述中不正确的是( )
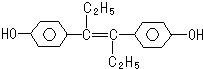

| A、该有机物分子中,至少8个碳原子一定共平面 |
| B、可与NaOH和NaHCO3发生反应 |
| C、1mol该有机物可以与5mol Br2发生反应 |
| D、它易溶于有机溶剂 |
用括号内的试剂和方法除去下列各种物质的少量杂质,不正确的是( )
| A、苯中含有苯酚(浓溴水,过滤) |
| B、乙酸钠中含有碳酸钠(乙酸,蒸发) |
| C、乙酸乙酯中含有乙酸(饱和碳酸钠溶液,分液) |
| D、溴乙烷中含有醇(水,分液) |
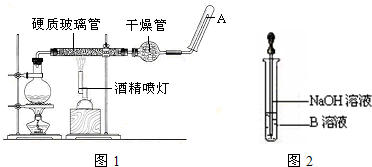
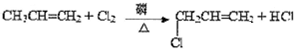
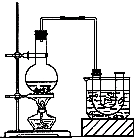 已知:CH3CH2OH+NaBr+H2SO4(浓)
已知:CH3CH2OH+NaBr+H2SO4(浓)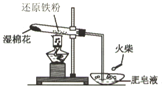 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验.
为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验.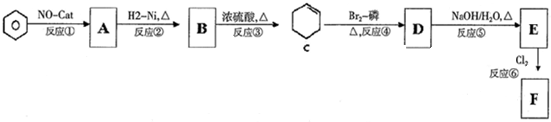
 F的结构简式为
F的结构简式为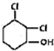
 直接制
直接制 ,理由是
,理由是