几种短周期元素的原子半径及主要化合价如表:下列叙述错误的是( )
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A、R的氧化物对应的水化物可能具有两性 |
| B、X单质在氧气中燃烧不可能生成XO3 |
| C、离子半径大小:r(M3+)>r(T2-) |
| D、L2+和X2-的核外电子数相等 |
根据原子结构及元素周期律的知识,下列推断正确的是( )
A、
| ||||
| B、同主族元素含氧酸的酸性随核电荷数的增加而减弱 | ||||
| C、Cl-、S2-、Ca2+、K+半径逐渐减小 | ||||
| D、核外电子排布相同的微粒化学性质也相同 |
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10;X原子和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强,下列说法正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10;X原子和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强,下列说法正确的是( )| A、对应简单离子半径:X>W>Y>Z |
| B、Y的氧化物能与Z或X的最高价氧化物对应的水化物反应 |
| C、X、W两元素形成的二元化合物中一定含有离子键 |
| D、对应气态氢化物的稳定性W>Y,对应气态氢化物的熔沸点Y>W |
已知短周期元素的离子.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A、原子半径 A>B>D>C |
| B、a-c=1 |
| C、离子半径 C>D>B>A |
| D、单质的还原性 A>B>D>C |
已知25℃时,氢氟酸的电离平衡常数KaHF=3.6×10-4,CaF2的溶度积常数Ksp(CaF2)=1.46×10-10,现向1L 0.2mol?L-1HF溶液中加入1L 0.2mol?L-1CaCl2溶液,则下列说法中,正确的是( )
| A、25℃时,0.1mol?L-1HF 溶液中pH=2 |
| B、Ksp(CaF2)随温度和浓度的变化而变化 |
| C、该体系中没有沉淀产生 |
| D、该体系中HF与CaCl2反应产生沉淀 |
下列说法正确的是( )
| A、HIO与HCN均为含有极性键的直线形极性分子 |
| B、SiO2与C02均为每摩含有4×6.02×1023对共用电子对的酸性氧化物 |
| C、Na2S浓溶液与稀盐酸分别滴加到饱和AgCl溶液中均一定有沉淀产生 |
| D、明矾与离子交换树脂均能将海水进行淡化 |
2.1g镁铝合金完全溶于足量盐酸,生成氢气2.24L(标准状况下),再向溶液中加入氢氧化钠溶液,生成沉淀的质量最大是( )
| A、2.9 g |
| B、4.6 g |
| C、5.5 g |
| D、6.9 g |
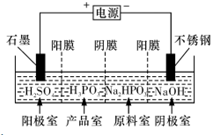 亚磷酸(H3P03 )是二元酸,H3 P03溶液中存在电离平衡:H3PO3?H-+H2PO3-亚磷酸与足量NaOH溶液反应,生成Na2 HPO3.
亚磷酸(H3P03 )是二元酸,H3 P03溶液中存在电离平衡:H3PO3?H-+H2PO3-亚磷酸与足量NaOH溶液反应,生成Na2 HPO3.