碘盐中添加的碘酸钾在工业上可用电解KI溶液制取,电极材料是石墨和不锈钢,化学方程式是:KI+3H2O
KIO3+3H2↑,有关说法不正确的是( )
| ||
| A、石墨作阳极,不锈钢作阴极 |
| B、I-在阳极放电,H+在阴极放电 |
| C、电解过程中电解质溶液的pH变小 |
| D、电解转移3 mol e-时,理论上可制得KIO3 107 g |
以石墨作电极电解下列溶液,电解后加入括号内的物质不能使电解质溶液恢复原状的是( )
| A、CuCl2溶液(CuCl2) |
| B、CuSO4溶液(CuO) |
| C、NaCl溶液(HCl) |
| D、KNO3溶液(KNO3) |
将蔗糖用少量水湿润后,一边搅拌一边加入浓硫酸.可以看到蔗糖颜色逐渐变黑,体积不断膨胀,最后变成多孔疏松固体.上述过程中,体现出浓硫酸( )
| A、只有吸水性 |
| B、只有脱水性 |
| C、既有吸水性.又有脱水性 |
| D、有脱水性、吸水性、氧化性 |
制备相同质量的硝酸铜,从经济效益和环保角度考虑,最适宜采用的方法是( )
| A、Cu+HNO3(浓)→Cu(NO3)2 | |||||
| B、Cu+HNO3(稀)→Cu(NO3)2 | |||||
| C、Cu+AgNO3→Cu(NO3)2 | |||||
D、Cu
|
将2.24L(标况下)的CO2和CO混合气体通有足量Na2O2固体的密闭容器中,同时不断地用电火花点燃,充分反应后剩余0.28L(标况下)的某气体,则原混合气体中CO2和CO的体积比为( )
| A、1:1 | B、1:3 |
| C、2:1 | D、1:4 |
相同质量的铜片分别与过量的体积相同的浓硝酸、稀硝酸反应.二者比较,相等的是(溶液体积变化忽略不计)( )
①铜片消耗完所需时间;
②反应生成的气体体积(标准状况);
③反应中氧化剂得到的电子总数;
④反应后溶液中铜离子的浓度.
①铜片消耗完所需时间;
②反应生成的气体体积(标准状况);
③反应中氧化剂得到的电子总数;
④反应后溶液中铜离子的浓度.
| A、①③ | B、②④ | C、③④ | D、只有① |
你认为下列行为中与“节能减排,和谐发展”不相符的是( )
| A、开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料 |
| B、将煤进行气化处理,提高煤的综合利用效率 |
| C、大量开采煤、石油,提高产量以满足工业生产的快速发展 |
| D、实现资源的“3R”利用观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle) |
甲、乙、丙都是金属单质,当电解甲离子和丙离子的混合盐溶液时,丙先析出,当甲与乙组成原电池时,甲为电池的正极,甲、乙、丙三种金属的活动性顺序为( )
| A、甲>乙>丙 |
| B、乙>甲>丙 |
| C、乙>丙>甲 |
| D、丙>乙>甲 |
下列生产、生活中的事实不能用金属活动性顺序表解释的是( )
| A、铝制器皿不宜盛放酸性食物 |
| B、电解食盐水时阴极产生氢气 |
| C、可用铁制容器盛放和运输浓硫酸 |
| D、镀锌铁桶镀层破损后铁仍不易被腐蚀 |
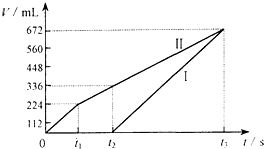 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算: