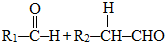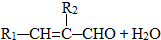题目内容
碘盐中添加的碘酸钾在工业上可用电解KI溶液制取,电极材料是石墨和不锈钢,化学方程式是:KI+3H2O
KIO3+3H2↑,有关说法不正确的是( )
| ||
| A、石墨作阳极,不锈钢作阴极 |
| B、I-在阳极放电,H+在阴极放电 |
| C、电解过程中电解质溶液的pH变小 |
| D、电解转移3 mol e-时,理论上可制得KIO3 107 g |
考点:电解原理
专题:
分析:A.根据电池反应式知,阳极上碘离子放电,则阳极为惰性电极;
B.电解时,阴极上氢离子放电,阳极上碘离子放电;
C.根据电解反应进行判断;
D.根据碘酸钾和转移电子之间的关系式计算.
B.电解时,阴极上氢离子放电,阳极上碘离子放电;
C.根据电解反应进行判断;
D.根据碘酸钾和转移电子之间的关系式计算.
解答:
解:A.根据电池反应式知,阳极上碘离子放电生成碘酸根离子,则阳极应该为惰性电极石墨,阴极为不锈钢,故A正确;
B.电解时,阴极上氢离子放电生成氢气,阳极上碘离子放电生成KIO3,故B正确;
C.碘化钾和碘酸钾都是强酸强碱盐,其溶液都呈中性,电解过程中水参加反应,导致溶液浓度增大,但pH几乎不变,故C错误;
D.KI和KIO3在酸性溶液中发生反应:KI+3H2O
KIO3+3H2↑,当电解过程中转移6mol e-时,理论上可制得1molKIO3,所以当电解过程中转移3 mol e-时,理论上可制得KIO3 107 g,故D正确;
故选:C.
B.电解时,阴极上氢离子放电生成氢气,阳极上碘离子放电生成KIO3,故B正确;
C.碘化钾和碘酸钾都是强酸强碱盐,其溶液都呈中性,电解过程中水参加反应,导致溶液浓度增大,但pH几乎不变,故C错误;
D.KI和KIO3在酸性溶液中发生反应:KI+3H2O
| ||
故选:C.
点评:本题考查了电解原理,根据电池反应式判断阴阳极材料、电极反应,并结合盐的性质分析解答,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
短周期元素R、T、X、Y、Z在元素周期表的相对位置如表所示,它们的核外电子数之和为58.则下列判断不正确的是( )
| R | T | |
| X | Y | Z |
| A、R的其中一种单质可用做电极材料 |
| B、五种元素中原子半径最大的是X |
| C、气态氢化物稳定性:Y>T |
| D、Z元素的最高价氧化物对应的水化物的化学式为HZO4 |
下列关于油脂的叙述不正确的是( )
| A、油脂是一种混合物 |
| B、油脂属于酯类 |
| C、油脂是高级脂肪酸甘油酯 |
| D、油脂都不能使溴水褪色 |
已知某镍镉(Ni-Cd)电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O
Cd(OH)2+2Ni(OH)2.有关该电池的说法正确的是( )
| 放电 |
| 充电 |
| A、充电时阳极的反应式为:Ni(OH)2-e-+OH-=NiOOH+H2O |
| B、充电时将镍镉电池的正极与外加直流电源的负极相连 |
| C、放电时负极附近溶液的碱性不变 |
| D、放电时电解质溶液中的OH-向正极移动 |
将2.24L(标况下)的CO2和CO混合气体通有足量Na2O2固体的密闭容器中,同时不断地用电火花点燃,充分反应后剩余0.28L(标况下)的某气体,则原混合气体中CO2和CO的体积比为( )
| A、1:1 | B、1:3 |
| C、2:1 | D、1:4 |
密度为0.91g/cm3的氨水,质量分数为25%.该氨水用等体积的水稀释后,所得溶液中溶质的质量分数( )
| A、等于12.5% |
| B、大于12.5% |
| C、小于12.5% |
| D、无法确定 |
下列实验中,能达到实验目的是( )
A、 排水法收集H2 |
B、 除去Cl2中HCl |
C、 分离碘和酒精 |
D、 比较Na2CO3与NaHCO3的热稳定性 |
工业上用制盐剩下的苦卤(主要成分是MgCl2)来制取硝酸镁,下列方案中合理可行的是( )
| A、向苦卤中加入AgNO3,滤出沉淀,将溶液蒸干 |
| B、将苦卤蒸发浓缩,再加入AgNO3,把得到的溶液蒸发结晶 |
| C、给苦卤中加入熟石灰,分离出沉淀,用稀硝酸将沉淀溶解,再将溶液浓缩结晶 |
| D、将苦卤浓缩结晶,再进行电解,得到金属镁,用镁和HNO3反应 |
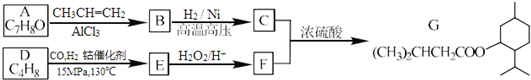
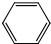 +CH2=CH2
+CH2=CH2