题目内容
制备相同质量的硝酸铜,从经济效益和环保角度考虑,最适宜采用的方法是( )
| A、Cu+HNO3(浓)→Cu(NO3)2 | |||||
| B、Cu+HNO3(稀)→Cu(NO3)2 | |||||
| C、Cu+AgNO3→Cu(NO3)2 | |||||
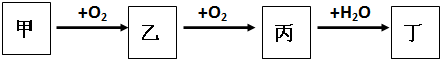
D、Cu
|
考点:铜金属及其重要化合物的主要性质
专题:元素及其化合物
分析:制备相同质量的硝酸铜,从经济效益和环保角度考虑,需要的物质越少越好且反应过程中不产生有毒气体,以此来解答.
解答:
解:A.铜和浓硝酸反应生成NO2,二氧化氮有毒,污染空气,故A不选;
B.铜和稀硝酸反应生成NO,NO有毒,污染空气,故B不选;
C.铜和硝酸银反应生成硝酸铜,但硝酸银价格较昂贵,不经济,故C不选;
D.该过程中不产生有毒气体,且使用材料较廉价,符合条件,故D选;
故选D.
B.铜和稀硝酸反应生成NO,NO有毒,污染空气,故B不选;
C.铜和硝酸银反应生成硝酸铜,但硝酸银价格较昂贵,不经济,故C不选;
D.该过程中不产生有毒气体,且使用材料较廉价,符合条件,故D选;
故选D.
点评:本题考查硝酸铜的制备,为高频考点,把握制备原理及物质的性质为解答的关键,侧重物质制备的评价性分析,注意原料及环保角度分析,明确常见的有毒气体,题目难度不大.

练习册系列答案
相关题目
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
| A、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1 452 kJ?mol-1 |
| B、CH3OH(l)+1.5O2(g)=CO2(g)+2H2O(g)△H=-725.8 kJ?mol-1 |
| C、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-725.8 kJ?mol-1 |
| D、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=+1 452 kJ?mol-1 |
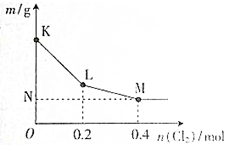 向100mlNaBr和NaI的混合溶液中慢慢通入Cl2(假设Cl2全部反应),使其充分反应后,将所得溶液蒸干、灼烧、得到的固体的质量为m,m与通入的n(Cl2)的关系如图所示,下列说法正确的是( )
向100mlNaBr和NaI的混合溶液中慢慢通入Cl2(假设Cl2全部反应),使其充分反应后,将所得溶液蒸干、灼烧、得到的固体的质量为m,m与通入的n(Cl2)的关系如图所示,下列说法正确的是( )| A、K→L段发生反应的离子方程式为2Br-+Cl2═2Cl-+Br2 |
| B、原溶液中,c(Na+ )=4mol?L-1 |
| C、原溶液中,c(I-)=2mol?L-1 |
| D、M点代表的固体质量为46.8g |
下列生产、生活中的事实不能用金属活动性顺序表解释的是( )
| A、铝制器皿不宜盛放酸性食物 |
| B、电解食盐水时阴极产生氢气 |
| C、可用铁制容器盛放和运输浓硫酸 |
| D、镀锌铁桶镀层破损后铁仍不易被腐蚀 |
在醋酸溶液中,加入下列物质不影响醋酸电离平衡的是 ( )
| A、Na |
| B、CaCO3 |
| C、BaCl2 |
| D、NaHSO4 |
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池反应为:2CH3OH+3O2+4OH-
2CO32-+6H2O则下列说法正确的是( )
| 充电 |
| 放电 |
| A、构成该电池的正极和负极必须是两种活性不同的金属 |
| B、充电时有CH3OH生成的电极为阳极 |
| C、放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O |
| D、充电时每生成1 mol CH3OH转移12mol电子 |
把铁和铜加入到氯化铁、氯化亚铁和氯化铜的混合溶液中,反应后铁有剩余则( )
| A、溶液中有Fe2+、Cu2+ |
| B、剩下的固体是Fe和Cu |
| C、溶液中有Fe3+、Fe2+ |
| D、剩下的固体是Fe,无Cu |