在密闭容器中进行反应:2A(g)+B(g)?3C(g)△H>0.下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
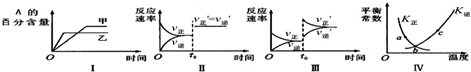

| A、图I表示温度对化学平衡的影响,且甲的温度较高 |
| B、图Ⅱ表示t0时刻缩小容器体积对反应速率的影响 |
| C、图Ⅲ表示t0时刻增大B浓度对反应速率的影响 |
| D、图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |
密闭容器中的平衡体系H2+I2(g)?2HI(g)△H<O,欲使HI浓度增大,可采取的措施是( )
| A、扩大体积 | B、升温 |
| C、降温 | D、加催化剂 |
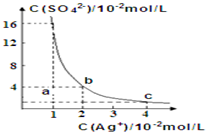 某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:下列有关Ag2SO4说法正确的是( )
某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:下列有关Ag2SO4说法正确的是( )| A、含有大量SO42-的溶液中肯定不存在Ag+ |
| B、Ag2SO4的溶度积常数(Ksp)为8×10-4 |
| C、a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
| D、0.02mol?L-1的AgNO3溶液与0.2mol?L-1的Na2SO4溶液等体积混合不会生成沉淀 |
把Ca(OH)2放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2(s)?Ca2+(aq)+2OH-(aq).当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是( )
| A、溶液中Ca2+的浓度增大 |
| B、溶液中Ca2+的浓度减小 |
| C、溶液中pH不变 |
| D、溶液中pH增大 |
 回答下列问题:
回答下列问题: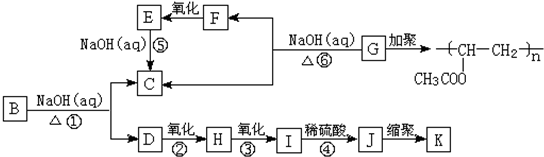


 也能发生类似V→I的反应,请写出生成醇的结构简式
也能发生类似V→I的反应,请写出生成醇的结构简式