下列有关C、N、S等非金属元素化合物的说法正确的是( )
| A、NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
| B、SO2具有漂白性可以是酸性高锰酸钾溶液褪色 |
| C、实验室可用NaOH溶液处理NO2和SO2废气 |
| D、稀硝酸、稀硫酸均能将木炭氧化成二氧化碳 |
可以验证硫元素的非金属性比氯元素弱的事实是( )
①硫和氢气在加热条件下能形成H2S、H2S受热300℃左右分解.氯气和氢气在点燃或光照下生成氯化氢,氯化氢很难分解;
②向氢硫酸溶液中滴入氯水有单质硫生成;
③硫、氯气分别与铜和铁反应产物是 FeS、Cu2S、FeCl3、CuCl2;
④高氯酸(HClO4)的酸性强于硫酸;
⑤盐酸酸性强于氢硫酸.
①硫和氢气在加热条件下能形成H2S、H2S受热300℃左右分解.氯气和氢气在点燃或光照下生成氯化氢,氯化氢很难分解;
②向氢硫酸溶液中滴入氯水有单质硫生成;
③硫、氯气分别与铜和铁反应产物是 FeS、Cu2S、FeCl3、CuCl2;
④高氯酸(HClO4)的酸性强于硫酸;
⑤盐酸酸性强于氢硫酸.
| A、①②③④ | B、只有①② |
| C、只有②③④ | D、①②③④⑤ |
下列物质长期露置在空气中不易变质的是( )
| A、漂白粉 | B、苯酚 |
| C、水玻璃 | D、碳酸钠粉末 |
室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是( )
| A、0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液 |
| B、0.1mol/L的盐酸和0.1mol/L的氢氧化钡溶液 |
| C、pH=4的醋酸溶液和pH=10的氢氧化钠溶液 |
| D、pH=4的盐酸和pH=9的氨水 |
根据酸碱质子理论,凡是能给出质子的分子或离子都是酸,凡是能结合质子的分子或离子都是碱.按照这个理论,下列微粒属于两性物质的是( )
| A、HCO3- |
| B、CO32- |
| C、Fe(OH)3 |
| D、CH3COOH |
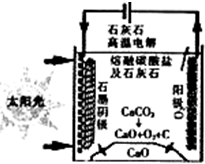 资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.
资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.