题目内容
常温下,有四种溶液:
回答下列问题:
(1)①稀释到原来的10倍后的溶液pH (填“>”“=”或“<”,下同)④溶液的pH,①和③两溶液中水电离出的c(H+):① ③.
(2)若①和②混和所得溶液中离子浓度大小为c(Na+)>c(CH3COO-)>c(OH-)>c(H+),其溶液中电荷守恒式为 .
(3)①与③混合,若溶液pH=7,则两溶液体积关系为 V(NaOH) V(CH3COOH).
(4)②与④混合,若溶液显酸性,则溶液中的c(Na+) c(CH3COO-),其所得溶液中的溶质组成可能为 .
| ① | ② | ③ | ④ |
| 0.1mol?L-1 CH3COOH 溶液 | pH=12 NaOH溶液 | 0.1mol?L-1 NaOH 溶液 | pH=2 CH3COOH 溶液 |
(1)①稀释到原来的10倍后的溶液pH
(2)若①和②混和所得溶液中离子浓度大小为c(Na+)>c(CH3COO-)>c(OH-)>c(H+),其溶液中电荷守恒式为
(3)①与③混合,若溶液pH=7,则两溶液体积关系为 V(NaOH)
(4)②与④混合,若溶液显酸性,则溶液中的c(Na+)
考点:酸碱混合时的定性判断及有关ph的计算,pH的简单计算
专题:
分析:(1)0.1mol/L CH3COOH溶液,稀释10倍醋酸浓度为0.01mol/L,c(H+)<<0.01mol/L,溶液PH>>4,pH=4的CH3COOH溶液中氢离子浓度10-4mol/L稀释10倍,促进电离,pH小于5; ④pH=4的CH3COOH溶液中水电离出的氢离子浓度为10-10mol/L,⑤pH=4NH4Cl溶液两溶液中水电离出的c(H+)为10-4mol/L;
(2)溶液中阴离子和阳离子所带电荷数相同书写得到;
(3)①与③混合,若溶液pH=7,依据醋酸和氢氧化钠恰好反应生成醋酸钠,溶液呈碱性,若成中性醋酸略过量分析;
(4)②pH=10NaOH溶液与④pH=4CH3COOH溶液等体积混合,醋酸电离平衡状态下的氢离子浓度和氢氧化钠溶液中的氢氧根离子浓度相同,等体积混合恰好反应,醋酸是弱电解质,电离平衡正向进行,又电离出氢离子,醋酸溶液浓度大于氢氧化钠溶液,说明反应后溶液为醋酸和醋酸钠.
(2)溶液中阴离子和阳离子所带电荷数相同书写得到;
(3)①与③混合,若溶液pH=7,依据醋酸和氢氧化钠恰好反应生成醋酸钠,溶液呈碱性,若成中性醋酸略过量分析;
(4)②pH=10NaOH溶液与④pH=4CH3COOH溶液等体积混合,醋酸电离平衡状态下的氢离子浓度和氢氧化钠溶液中的氢氧根离子浓度相同,等体积混合恰好反应,醋酸是弱电解质,电离平衡正向进行,又电离出氢离子,醋酸溶液浓度大于氢氧化钠溶液,说明反应后溶液为醋酸和醋酸钠.
解答:
解:(1)0.1mol/L CH3COOH溶液,稀释10倍醋酸浓度为0.01mol/L,c(H+)<<0.01mol/L,溶液PH>>4,pH=4的CH3COOH溶液中氢离子浓度10-4mol/L稀释10倍,促进电离,PH小于5,所以①稀释到原来的10倍后的溶液pH>④溶液的pH;,①是弱酸,氢离子浓度小于0.1mol/L,③是氢氧化钠溶液,氢氧根离子浓度为0.1mol/,两溶液中水电离出的c(H+)①>③;
故答案为:>;>;
(2)溶液中阴离子和阳离子所带电荷数相同,若①和②混和所得溶液中离子浓度大小为c(Na+)>c(CH3COO-)>c(OH-)>c(H+),其溶液中电荷守恒式为:c(Na+)+c(H+)=c(CH3COO-)+c(OH-);
故答案为:c(Na+)+c(H+)=c(CH3COO-)+c(OH-);
(3)①0.001mol?L-1CH3COOH溶液与③0.001mol?L-1NaOH溶液混合,若溶液pH=7,醋酸和氢氧化钠恰好反应生成醋酸钠,溶液呈碱性,若成中性醋酸略过量,则两溶液体积关系为V(NaOH)<V(CH3COOH);
故答案为:<;
(4)②pH=10NaOH溶液与④pH=4CH3COOH溶液等体积混合,醋酸电离平衡状态下的氢离子浓度和氢氧化钠溶液中的氢氧根离子浓度相同,等体积混合恰好反应,醋酸是弱电解质,电离平衡正向进行,又电离出氢离子,醋酸溶液浓度大于氢氧化钠溶液,说明反应后溶液为醋酸和醋酸钠;
故答案为:<;CH3COOH和 CH3COONa.
故答案为:>;>;
(2)溶液中阴离子和阳离子所带电荷数相同,若①和②混和所得溶液中离子浓度大小为c(Na+)>c(CH3COO-)>c(OH-)>c(H+),其溶液中电荷守恒式为:c(Na+)+c(H+)=c(CH3COO-)+c(OH-);
故答案为:c(Na+)+c(H+)=c(CH3COO-)+c(OH-);
(3)①0.001mol?L-1CH3COOH溶液与③0.001mol?L-1NaOH溶液混合,若溶液pH=7,醋酸和氢氧化钠恰好反应生成醋酸钠,溶液呈碱性,若成中性醋酸略过量,则两溶液体积关系为V(NaOH)<V(CH3COOH);
故答案为:<;
(4)②pH=10NaOH溶液与④pH=4CH3COOH溶液等体积混合,醋酸电离平衡状态下的氢离子浓度和氢氧化钠溶液中的氢氧根离子浓度相同,等体积混合恰好反应,醋酸是弱电解质,电离平衡正向进行,又电离出氢离子,醋酸溶液浓度大于氢氧化钠溶液,说明反应后溶液为醋酸和醋酸钠;
故答案为:<;CH3COOH和 CH3COONa.
点评:本题考查了溶液酸碱性分析判断,溶液pH计算应用,注意酸碱反应后溶液酸碱性的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列化学方程式与所述事实相符,且正确的是( )
| A、检验燃尽的火柴头浸泡液中含有氯元素ClO3-+3NO2-+Ag+═AgCl↓+3NO3- |
| B、用淀粉碘化钾溶液和醋酸鉴别真假碘盐:IO3-+5I-+6H+=3I2+3H2O |
| C、用纸层析法分离Fe3+和Cu2+时,最后阶段充分氨熏:Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+ |
| D、在硫酸亚铁溶液中加入等物质的量的硫酸铵,制备摩尔盐FeSO4+(NH4)2SO4+6H2O═(NH4)2SO4?FeSO4?6H2O↓ |
NA代表阿伏伽德罗常数,下列叙述正确的是( )
| A、10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% |
| B、1molFe与过量的稀HNO3反应,转移的电子数为2 NA |
| C、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| D、一定温度下,l L 0.50 mol?L-1NH4C1溶液与2 L0.25mol?L-1NH4C1溶液NH4+的离子数均为0.5NA |
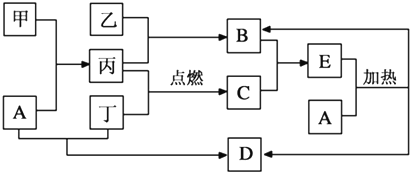
下列各组物质中,满足表中图示物质在通常条件下一步转化关系的组合只有( )
| 序号 | X | Y | Z | W |  |
| ① | CuO | Cu(OH)2 | CuSO4 | Cu | |
| ② | NaCl | NaHCO3 | Na2CO3 | NaOH | |
| ③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
| ④ | SO2 | H2SO3 | Na2SO3 | NaHSO3 |
| A、①②③ | B、①③④ |
| C、②③④ | D、①②④ |
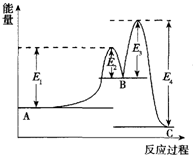 某反应由两步反应A→B→C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A→B→C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A、两步反应均为吸热反应 |
| B、加入催化剂会改变反应的焓变 |
| C、三种化合物中C最稳定 |
| D、A→C反应中△H=E1-E2 |
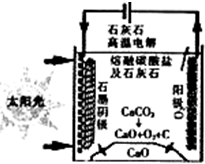 资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.
资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.