下列有关化学用语能表示甲烷的分子组成,但不能反映其分子空间构型的是( )
A、结构示意图: |
B、电子式: |
C、球棍模型: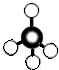 |
D、比例模型: |
已知,还原性I->Fe2+>Br-.向FeI2和FeBr2物质的量之比为1:1的混合溶液中逐滴滴入氯水,下列离子反应不可能发生的是( )
| A、2Fe2++4I-+3Cl2→2Fe3++2I2+6Cl- |
| B、2Fe2++2I-+2Cl2→2Fe3++I2+4Cl- |
| C、2Fe2++2I-+2Br-+3Cl2→2Fe3++I2+Br2+6Cl- |
| D、2Fe2++4I-+4Br-+5Cl2→2Fe3++2I2+2Br2+10Cl- |
下列化学反应对应的离子方程式书写正确的是( )
| A、醋酸溶液与Mg(OH)2反应:Mg(OH)2+2H+═Mg2++2H2O | ||||
| B、碳酸钠溶液呈碱性:CO32-+2H2O?H2CO3+2OH- | ||||
| C、NH4HC03溶液与过量NaOH溶液反应:NH4++OH-═NH3?H2O | ||||
D、用惰性电极电解饱和食盐溶液:2Cl-+2H2O
|
与事实吻合的离子方程式是( )
| A、加热可增强纯碱溶液的去污力:CO32-+2H2O═H2CO3+2OH-_Q(Q>0) |
| B、向Ca(HCO3)2(aq)中加入少量澄清石灰水出现白色沉淀:Ca2++OH-+HCO3-→CaCO3↓+H2O |
| C、Fe3O4溶于稀HNO3:Fe3O4+8H+→Fe2++2Fe3++4H2O |
| D、稀硝酸可洗去试管内壁的银镜:Ag+2H++NO3-→Ag++NO2↑+H2O |
下列说法正确的是( )
| A、任何化学反应都可以设计成电解池反应 |
| B、电镀铜和电解精炼铜时,电解质溶液中的c( Cu2+)均保持不变 |
| C、电解冶炼镁、铝通常电解MgCl2 和Al2O3,也可电解MgO和AlCl3 |
| D、若把Cu+H2SO4═CuSO4+H2↑ 设计成电解池,应用Cu作阳极 |
下列指定反应的离子方程式正确的是( )
| A、Na2SO3溶液中滴加稀H2SO4:SO32-+2H+=SO2↑+H2O |
| B、向AlCl3溶液中滴入足量的浓氨水:Al3++4OH-=AlO2-+2H2O |
| C、Ca(ClO)2溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32- |
| D、Fe(NO3)2溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
下列反应的离子方程式正确的是( )
| A、Fe3O4与稀硝酸反应:Fe3O4+8H+=Fe2++2Fe3++4H2O | ||||
| B、FeI2溶液中通入极少量Cl2:2I-+Cl2=I2+2Cl- | ||||
C、用惰性电极电解饱和氯化镁溶液:2Cl-+2H2O
| ||||
| D、Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |