常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
| A、Ca(ClO)2溶液中:c(Ca2+)>c(ClO-)>c(OH-)>c(H-) |
| B、等体积、等物质的量浓度的Na2SO3溶液与NaHSO3溶液混合:c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) |
| C、将0.2mol.L-1的某一元酸HA溶液和0.1mol.L-1的NaOH溶液等体积混合后溶液的pH大于7,则反应后的混合液:2c(OH-)+c(A-)=2c(H+)+c(HA) |
| D、某溶液中水电离出的c(OH-)=1×10-amol.L-1若a>7时,则pH该溶液的一定为14-a |
已知某溶液中存在较多的H+、SO42-、NO3-,则该溶液中还可能大量存在的离子组是( )
| A、Na+、CO32-、Cl- |
| B、Mg2+、Ba2+、Br- |
| C、Ag+、Na+、Cl- |
| D、Na+、NH4+、Cl- |
W、X、Y、Z是核外电子层数相同且原子序数依次增大的短周期元素,W、X是金属元素,Y的氢化物为H2Y,Z的某种含氧酸有漂白性.W、X的最高价氧化物对应的水化物可以发生反应生成盐和水.下列判断正确的是( )
| A、X的金属性强于W的金属性 |
| B、W、X分别与Z形成的化合物都是离子化合物 |
| C、W、X、Y、Z的简单离子的半径:Y>Z>W>X |
| D、Y的氧化物通入含有Z单质的溶液中,一定无明显变化 |
四种短周期元素W、X、Y、Z原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,X2+和Z-离子的电子数之差为8,下列说法正确的是( )
| A、与W相邻的同主族元素单质的重要用途是制作光纤 |
| B、X单质不可能置换出W单质 |
| C、元素原子半径从大到小的顺序是X、Y、Z |
| D、由非金属性强弱可知,不可能由W的含氧酸制备Z的含氧酸 |



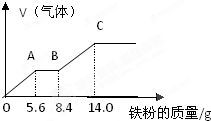 某稀硫酸和稀硝酸的混合溶液100mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸的还原产物只有NO气体)
某稀硫酸和稀硝酸的混合溶液100mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸的还原产物只有NO气体)