a、b、c、d是四种短周期元素.a、b、d同周期,c、d同主族.a的原子结构示意图为  ,b与c形成化合物的电子式
,b与c形成化合物的电子式  为下列比较中正确的是( )
为下列比较中正确的是( )
 ,b与c形成化合物的电子式
,b与c形成化合物的电子式  为下列比较中正确的是( )
为下列比较中正确的是( )| A、原子半径:a>c>d>b |
| B、电负性:a>b>d>c |
| C、最高价含氧酸的酸性:c>d>a |
| D、第一电离能:d>a>b>c |
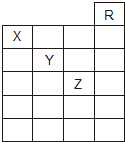 如图是元素周期表前六周期的一部分,关于元素X、Y、Z的叙述正确的是( )
如图是元素周期表前六周期的一部分,关于元素X、Y、Z的叙述正确的是( )①X的气态氢化物与Y最高价氧化物对应的水化物能发生反应生成盐
②X、Y、Z的气态氢化物的水溶液的酸性X<Y<Z
③Z的单质常温下是液体,可与铁粉反应
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素.
| A、只有③ | B、只有①④ |
| C、只有①②③④ | D、①②③④⑤ |
可能存在的第119号未知元素,有人称为“类钫”,根据周期表结构及元素性质变化趋势,有关“类钫”的预测,说法不正确的是( )
| A、“类钫”在化合物中是+1价 |
| B、“类钫”具有放射性 |
| C、“类钫”单质的密度大于l g?cm-3 |
| D、“类钫”单质有较高的熔点 |
如表为元素周期表中短周期的一部分.下列有关A、B、C、D、E五种元素的叙述中,不正确的是( )

| A、A与B形成的阴离子可能有:AB32-、A2B42- |
| B、E的氢化物的沸点比C的氢化物的沸点高 |
| C、D在过量的B中燃烧的主要产物为DB2 |
| D、A与E形成的化合物是非极性分子 |
 海水中含有丰富的锂资源,研究人员开发了一种只能让锂离子通过的特殊交换膜,并运用电解实现从海水中提取高浓度的锂盐,其工作原理如图所示.下列说法不正确的是( )
海水中含有丰富的锂资源,研究人员开发了一种只能让锂离子通过的特殊交换膜,并运用电解实现从海水中提取高浓度的锂盐,其工作原理如图所示.下列说法不正确的是( )| A、a 连接电源的正极 |
| B、Li+的移动方向是从海水进入到盐酸中 |
| C、过程中还可能获得有经济价值的副产物氢气和氯气 |
| D、一段时间后,b电极附近溶液的pH降低 |
 某温度下的溶液中c(H+)=1.0×10 x mol/L,c(OH-)=1.0×10 y mol/L.x与y的关系如图所示.请回答下列问题:
某温度下的溶液中c(H+)=1.0×10 x mol/L,c(OH-)=1.0×10 y mol/L.x与y的关系如图所示.请回答下列问题: