下列说法正确的是( )
A、MgCl2的形成过程可表示为 → → |
| B、H2O分子的结构式可表示为H-O-H |
| C、NaOH是离子化合物,所以不含共价键 |
D、Na2S的电子式为: |
不同温度(T1和T2)时,硫酸钡在水中的沉淀溶解平衡曲线如图所示,已知硫酸钡在水中溶解时吸收热量.下列说法正确的是( )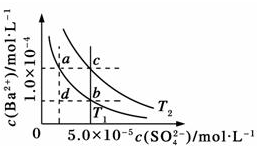

| A、T1>T2 |
| B、加入BaCl2固体,可使a点变成c点 |
| C、c点时,在T1、T2两个温度下均有固体析出 |
| D、a点和b点的Ksp相等 |
金刚石和石墨两种晶体中,每个最小的碳环里实际所包含的碳原子数( )
| A、前者多 | B、后者多 |
| C、相等 | D、无法确定 |

 的合成路线(合成路线常用的表示方法为:A
的合成路线(合成路线常用的表示方法为:A

