题目内容
饱和烃A和不饱和烃B在常温下均为气体,其中A含的碳原子数多于B.
(1)将A、B按一定比例混合,1 L混合气体完全燃烧后在同温同压下得到3.6 LCO2,试推断该混合气体的可能组成及A、B混合时的体积比 .
(2)1 mol该混合气体恰好能使含0.4 mol溴的四氯化碳溶液完全褪色,推断上述各组合中符合该条件的A和B的化学式 .
(3)120℃时,1 L A和1 L B与足量O2混合后点燃,在同温同压下体积增大2L,试通过计算确定A和B的化学式 .
(1)将A、B按一定比例混合,1 L混合气体完全燃烧后在同温同压下得到3.6 LCO2,试推断该混合气体的可能组成及A、B混合时的体积比
(2)1 mol该混合气体恰好能使含0.4 mol溴的四氯化碳溶液完全褪色,推断上述各组合中符合该条件的A和B的化学式
(3)120℃时,1 L A和1 L B与足量O2混合后点燃,在同温同压下体积增大2L,试通过计算确定A和B的化学式
考点:有关有机物分子式确定的计算
专题:
分析:(1)根据体积之比等于物质的量之比,由混合气体1L充分燃烧后得到同温同压下3.6LCO2,可知混合气体的平均分子式为C3.6Hx,然后根据要想碳原子的平均值为3.6,必须有一种烃的碳原子数小于3.6,另一种烃的碳原子数大于3.6,且碳原子数若>4,那么常温下不是气体,故一种烃中最多为4个碳,据此讨论即可;
(2)
(3)
(2)
(3)
解答:
解:(1)因1升混合气体充分燃烧后生成3.6升CO2,且A分子的碳原子数比B分子的多,混合气体只能由碳原子数大于3.6的烷烃(C4H10)和碳原子数小于3.6的烯烃或炔烃(C3H6和C2H4、C3H4和C2H2)组成.它们有四种可能的组合:C4H10、C3H6;C4H10、C2H4;C4H10、C3H4;C4H10、C2H2;根据每一种组合中烷烃和烯烃的碳原子数及燃烧后生成的CO2体积,可确定A和B的体积比.如: ,则V(C4H10):V(C2H4)=4:1,依此类推,故答案为:①C4H10、C3H6、3:2;②C4H10、C2H4、4:1③C4H10、C2H2、4:1④C4H10、C3H4、3:2;
,则V(C4H10):V(C2H4)=4:1,依此类推,故答案为:①C4H10、C3H6、3:2;②C4H10、C2H4、4:1③C4H10、C2H2、4:1④C4H10、C3H4、3:2;
(2)如果是炔烃与溴水加成,炔应为0.2mol,因此炔烃与溴的物质的量之比为1:2,如果是烯烃与溴水加成,.即烯烃应为0.4mol,烯烃与溴水物质的量之比为1:1,故答案为:A:C4H10;B:C2H2;或A:C4H10;B:C3H6;
(3)设1升气态烃与氧充分燃烧后体积变化为△V升,则
CxHy+(x+
y)O2
CO2+
yH2O(气)△V
1 x+
y 1
y
y-1
2L 2L
=
,解y=8,平均分子式中H原子为8个,
故组合①符合题意,即A:C4H10;B:C3H6,故答案为:A:C4H10;B:C3H6.
 ,则V(C4H10):V(C2H4)=4:1,依此类推,故答案为:①C4H10、C3H6、3:2;②C4H10、C2H4、4:1③C4H10、C2H2、4:1④C4H10、C3H4、3:2;
,则V(C4H10):V(C2H4)=4:1,依此类推,故答案为:①C4H10、C3H6、3:2;②C4H10、C2H4、4:1③C4H10、C2H2、4:1④C4H10、C3H4、3:2;(2)如果是炔烃与溴水加成,炔应为0.2mol,因此炔烃与溴的物质的量之比为1:2,如果是烯烃与溴水加成,.即烯烃应为0.4mol,烯烃与溴水物质的量之比为1:1,故答案为:A:C4H10;B:C2H2;或A:C4H10;B:C3H6;
(3)设1升气态烃与氧充分燃烧后体积变化为△V升,则
CxHy+(x+
| 1 |
| 4 |
| 点燃 |
| 1 |
| 2 |
1 x+
| 1 |
| 4 |
| 1 |
| 2 |
| 1 |
| 4 |
2L 2L
| 1 | ||
|
| ||
| 2L |
故组合①符合题意,即A:C4H10;B:C3H6,故答案为:A:C4H10;B:C3H6.
点评:本题主要考查了十字交叉法、差量法的使用,有一定的难度,注意根据燃烧的方程式进行判断.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
下列说法正确的是( )
| A、离子化合物中可以含有共价键 |
| B、共价化合物中可以含有离子键 |
| C、当元素处于最高价态时一定具有强氧化性 |
| D、元素的性质呈周期性变化的根本原因是元素原子的核外电子排布呈周期性变化 |
不同温度(T1和T2)时,硫酸钡在水中的沉淀溶解平衡曲线如图所示,已知硫酸钡在水中溶解时吸收热量.下列说法正确的是( )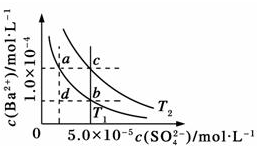

| A、T1>T2 |
| B、加入BaCl2固体,可使a点变成c点 |
| C、c点时,在T1、T2两个温度下均有固体析出 |
| D、a点和b点的Ksp相等 |
下列物质中既能跟氢气反应,又能跟KMnO4酸性溶液反应;既不能跟溴水反应,又不能发生加聚反应的是( )
| A、裂化汽油 | B、甲苯 |
| C、聚乙烯 | D、苯 |
下列物质既能发生消去反应,又能氧化成醛的是( )
| A、CH3CH2CH2OH |
| B、(CH3)2CHCH2OH |
| C、CH3OH |
D、 |
电渗析法是指在外加电场作用下,利用阴离子交换膜和阳离子交换膜的选择透过性,使部分离子透过离子交换膜而迁移到另一部分水中,从而使一部分水淡化而另一部分水浓缩的过程.如图是利用电渗析法从海水中获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为石墨电极.
下列有关描述错误的是( )
下列有关描述错误的是( )

| A、阳离子交换膜是A,不是B |
| B、通电后阳极区的电极反应式:2Cl--2e-→Cl2↑ |
| C、工业上阴极使用铁丝网代替石墨碳棒,以减少石墨的损耗 |
| D、阴极区的现象是电极上产生无色气体,溶液中出现少量白色沉淀 |
