0 108664 108672 108678 108682 108688 108690 108694 108700 108702 108708 108714 108718 108720 108724 108730 108732 108738 108742 108744 108748 108750 108754 108756 108758 108759 108760 108762 108763 108764 108766 108768 108772 108774 108778 108780 108784 108790 108792 108798 108802 108804 108808 108814 108820 108822 108828 108832 108834 108840 108844 108850 108858 203614


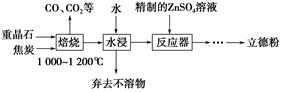
 BaS(s)+4CO2(g),该反应的平衡常数的表达式为__________________________________________________。
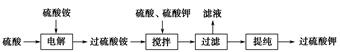
BaS(s)+4CO2(g),该反应的平衡常数的表达式为__________________________________________________。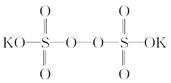 )具有强氧化性(常被还原为硫酸钾),80 ℃以上易发生分解。实验室模拟工业合成过硫酸钾的流程如下:
)具有强氧化性(常被还原为硫酸钾),80 ℃以上易发生分解。实验室模拟工业合成过硫酸钾的流程如下: