题目内容
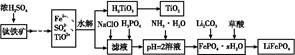
从海水中提取镁的工艺流程如图所示。

下列说法错误的是( )。

下列说法错误的是( )。
| A.用此法提取镁的优点之一是原料来源丰富 |
| B.步骤⑦电解MgCl2时阴极产生氯气 |
| C.步骤⑥可将晶体置于HCl气氛中脱水 |
| D.上述工艺流程中涉及化合、分解和复分解反应 |
B
用此法提取镁的原料为海水和贝壳,来源丰富,价格低廉,A项正确;电解MgCl2时,阴极上产生的是Mg,阳极上产生的应是氯气,B项错误;将MgCl2·6H2O晶体置于HCl气氛中脱水,可以抑制MgCl2发生水解,得到较纯的MgCl2,C项正确;整个工艺流程发生的化学反应方程式为:CaCO3 CaO+CO2↑,CaO+H2O=Ca(OH)2,Mg2++2OH-=Mg(OH)2↓,Mg(OH)2+2HCl+4H2O=MgCl2·6H2O,MgCl2·6H2O
CaO+CO2↑,CaO+H2O=Ca(OH)2,Mg2++2OH-=Mg(OH)2↓,Mg(OH)2+2HCl+4H2O=MgCl2·6H2O,MgCl2·6H2O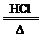 MgCl2+6H2O,MgCl2
MgCl2+6H2O,MgCl2 Mg+Cl2↑,涉及到化合、分解和复分解反应,D项正确。
Mg+Cl2↑,涉及到化合、分解和复分解反应,D项正确。
 CaO+CO2↑,CaO+H2O=Ca(OH)2,Mg2++2OH-=Mg(OH)2↓,Mg(OH)2+2HCl+4H2O=MgCl2·6H2O,MgCl2·6H2O
CaO+CO2↑,CaO+H2O=Ca(OH)2,Mg2++2OH-=Mg(OH)2↓,Mg(OH)2+2HCl+4H2O=MgCl2·6H2O,MgCl2·6H2O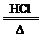 MgCl2+6H2O,MgCl2
MgCl2+6H2O,MgCl2 Mg+Cl2↑,涉及到化合、分解和复分解反应,D项正确。
Mg+Cl2↑,涉及到化合、分解和复分解反应,D项正确。
练习册系列答案
相关题目