题目内容
8.2015年2月,科学家首次观测到化学键的形成.下列粒子之间存在化学键的是( )| A. | 质子与电子之间 | B. | 水分子与水分子之间 | ||
| C. | 氧分子中氧原子与氧原子之间 | D. | 氯化钠中钠离子与钠离子之间 |
分析 化学键是原子或离子之间强烈的相互作用,化学键包括共价键、离子键和金属键,分子之间不存在化学键,存在范德华力或氢键,以此解答该题.
解答 解:A.化学键是原子或离子之间强烈的相互作用,质子与电子之间不存在化学键,故A不选;
B.分子之间不存在化学键,存在范德华力或氢键,故B不选;
C.氧分子中氧原子与氧原子之间存在共价键,故C选;
D.氯化钠中钠离子与氯离子之间存在离子键,钠离子与钠离子之间没有化学键,故D不选.
故选C.
点评 本题考查化学键,涉及化学键类型,为高考常见题型,侧重于学生的分析能力的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.膦(PH3)在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含之.它的分子是三角锥形.以下关于PH3的叙述中,正确的是( )
| A. | PH3是非极性分子 | |
| B. | PH3分子中有未成键的电子对 | |
| C. | PH3中的P-H键的极性比NH3中N-H键的极性弱 | |
| D. | PH3分子中的P-H键是非极性键 |
16.H2O、BF3 的杂化类型分别是( )
| A. | sp3、sp2 | B. | sp3、sp | C. | sp2、sp | D. | sp2、sp3 |
3.山西被称为煤海,欲提高煤的燃烧效率,下列说法正确的是( )
| A. | 将煤粉碎后燃烧 | B. | 通入大量的空气 | ||
| C. | 加入的煤越多越好 | D. | 将煤和空气在密闭的空间里燃烧 |
13.下列描述中正确的是( )
| A. | ClO3-的空间构型为平面三角形 | |
| B. | 乙炔分子中的两个碳原子采用sp2杂化方式 | |
| C. | CS2为V形的极性分子 | |
| D. | SiF4和SO32-的中心原子均为sp3杂化 |
20.下列说法正确的是(NA为阿伏加德罗常数)( )
| A. | 124 g P4含有P-P键的个数为4NA | |
| B. | 60gSiO2中含Si-O键的个数为2NA | |
| C. | 12 g石墨中含有C-C键的个数为1.5NA | |
| D. | 36 g戊烷中共价键的个数为10NA |
17.用括号中的试剂除去各组中的杂质,正确的是( )
| A. | 苯中的甲苯(溴水) | B. | 溴苯中的溴(苯) | ||
| C. | 乙烷中的乙烯(酸性高锰酸钾) | D. | 95.6%乙醇中的水(生石灰) |
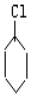 $→_{②}^{NaOH、乙醇}$
$→_{②}^{NaOH、乙醇}$ $→_{③}^{溴的CCl_{4}溶液}$B$\stackrel{④}{→}$
$→_{③}^{溴的CCl_{4}溶液}$B$\stackrel{④}{→}$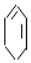

 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O.
+2NaBr+2H2O.