题目内容
17.用括号中的试剂除去各组中的杂质,正确的是( )| A. | 苯中的甲苯(溴水) | B. | 溴苯中的溴(苯) | ||
| C. | 乙烷中的乙烯(酸性高锰酸钾) | D. | 95.6%乙醇中的水(生石灰) |
分析 A.苯和甲苯都不与溴反应,且混溶;
B.苯与溴苯混溶;
C.乙烯被氧化生成二氧化碳;
D.水可与生石灰反应.
解答 解:A.苯和甲苯都不与溴反应,且混溶,不能用溴水除杂,故A错误;
B.苯与溴苯混溶,加入苯,不能除去溴,应加入氢氧化钠溶液,故B错误;
C.乙烯被氧化生成二氧化碳,引入新杂质,应用溴水除杂,故C错误;
D.水可与生石灰反应,然后蒸馏可得到乙醇,故D正确.
故选D.
点评 本题考查物质分离提纯方法的选择和应用,为高频考点,把握物质的性质及性质差异为解答的关键,侧重混合物除杂的考查,题目难度不大.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
7.X2+和Y-与氩的电子层结构相同,下列判断中正确的是( )
| A. | 原子半径X<Y | |
| B. | 离子半径 X2+<Y- | |
| C. | X与Y的原子序数之差为8 | |
| D. | 在元素周期表中,两者处于同一周期 |
8.2015年2月,科学家首次观测到化学键的形成.下列粒子之间存在化学键的是( )
| A. | 质子与电子之间 | B. | 水分子与水分子之间 | ||
| C. | 氧分子中氧原子与氧原子之间 | D. | 氯化钠中钠离子与钠离子之间 |
5.从经济效益和环境保护的角度考虑,大量制取硝酸铜最宜采用的方法是( )
| A. | Cu+HNO3(浓)→Cu(NO3)2 | |
| B. | Cu+HNO3(稀)→Cu(NO3)2 | |
| C. | Cu $\frac{空气}{加热}$ CuO $\frac{硝酸}{\;}$ Cu(NO3)2 | |
| D. | Cu $\frac{浓硫酸}{加热}$ CuSO4 $\frac{硝酸钡}{\;}$ Cu(NO3)2 |
12.在密闭容器中进行如下反应:X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A. | X2为0.2mol/L | B. | Y2为0.2mol/L | C. | Z为0.3mol/L | D. | Z为0.45mol/L |
9.将40g镁、铁、锌组成的混合物语适量的稀硫酸恰好完全反应,蒸干溶液测得固体质量136g,在上述溶液中加入一定量的氢氧化钠溶液使金属离子全部转化为沉淀,则此沉淀的质量是( )
| A. | 96g | B. | 74g | C. | 82.5g | D. | 无法计算 |
11.现有H2、CO(体积比为3:2)的混合气体a L,在相同条件下,当其完全燃烧时所需O2体积为( )
| A. | 0.5 a L | B. | a L | C. | 2 a L | D. | 3 a L |
12.10mLNO、CO2的混合气体通过足量的Na2O2后,气体的体积变为6mL(相同状况),则NO和CO2的体积比为( )
| A. | 1:1 | B. | 2:1 | C. | 3:2 | D. | 1:2 |
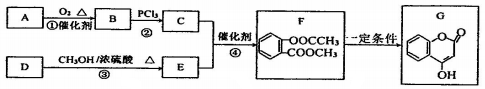
 +CH3COCl$\stackrel{催化剂}{→}$
+CH3COCl$\stackrel{催化剂}{→}$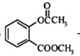 +HCl.
+HCl.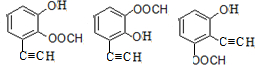 .
.