题目内容
18.设NA为阿伏伽德罗常数的值,下列说法正确的是( )| A. | 标准状况下,4.48L Cl2溶于水所得氯水中含氯的微粒总数为0.4NA | |
| B. | 5.6g乙烯和环丁烷(C4H8)的混合气体中含的碳原子数为0.4NA | |
| C. | 常温下,pH=2的盐酸溶液中含有的H+数目为0.02NA | |
| D. | 常温下,1L 0.5mol/L的FeCl3溶液中,所含Fe3+数为0.5NA |
分析 A.Cl2和H2O反应是可逆反应;
B.乙烯和环丁烷的实验式都是CH2;
C.缺少盐酸溶液的体积,无法计算;
D.Fe3+发生水解反应.
解答 解:A.标准状况下,4.48L Cl2含有0.2NA个分子,Cl2+H2O?H++Cl-+HClO,因此氯水中含氯的微粒总数小于0.4NA,故A错误;
B.N(C)=N(CH2)=$\frac{5.6g}{14g/mol}$×NAmol-1=0.4NA,故B正确;
C.缺少盐酸溶液的体积,无法计算H+数目,故C错误;
D.由于Fe3+发生水解反应,所以1L 0.5mol/L的FeCl3溶液中,所含Fe3+数小于0.5NA,故D错误;
故选B.
点评 本题考查阿伏伽德罗常数的计算,难度中等,涉及可逆反应、水解反应、实验式的应用,注意氯气和水反应是可逆反应.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
9.已知某反应是放热反应,下列说法正确的是( )
| A. | 该反应中反应物的总能量大于生成物的总能量 | |
| B. | 该反应中反应物的总能量小于生成物的总能量 | |
| C. | 该反应发生时,一定不需要加热 | |
| D. | 如果该反应开始后停止加热,反应一定能继续进行 |
6.下列物质中,不能作为干燥剂的是( )
| A. | 蓝色硫酸铜 | B. | 液体浓硫酸 | C. | 无水氯化钙 | D. | 白色碱石灰 |
13.关于乙酸的说法错误的是( )
| A. | 能与水互溶 | B. | 能与NaHCO3反应 | ||
| C. | 能发生酯化反应 | D. | 能与甲烷发生反应 |
3.下列各组离子在溶液中能大量共存的是( )
| A. | Fe3+、Cl-、NO3- | B. | K+、HCO3-、OH- | C. | Na+、HCO3-、H+ | D. | NH4+、H+、SO32- |
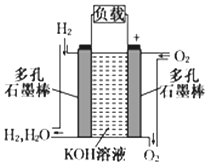 被誉为改变未来世界十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如下图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
被誉为改变未来世界十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如下图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题: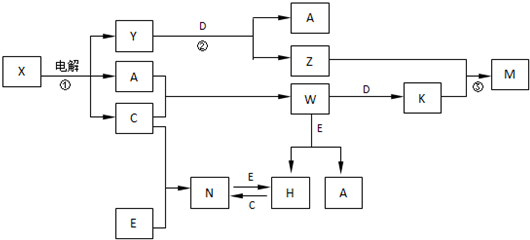
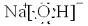 ,构成E单质的元素在周期表中位于第四周期第Ⅷ族.
,构成E单质的元素在周期表中位于第四周期第Ⅷ族.