题目内容
13.关于乙酸的说法错误的是( )| A. | 能与水互溶 | B. | 能与NaHCO3反应 | ||
| C. | 能发生酯化反应 | D. | 能与甲烷发生反应 |
分析 乙酸含-COOH,具有酸性,可发生酯化反应,不能与烷烃发生反应,以此来解答.
解答 解:A.含-COOH,与水分子可形成氢键,则乙酸易溶于水,故A正确;
B.含-COOH,能与NaHCO3反应生成二氧化碳,故B正确;
C.含-COOH,与醇可发生酯化反应,故C正确;
D.乙酸与甲烷不反应,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意羧酸的性质,题目难度不大.

练习册系列答案
相关题目
3.下列离子方程式正确的是( )
| A. | 醋酸溶液与新制氢氧化铜反应:2H++Cu(OH)2→Cu2++2H2O | |
| B. | 尼泊金酸与碳酸氢钠反应: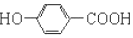 +2HCO3-→ +2HCO3-→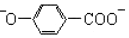 +2CO2↑+2H2O +2CO2↑+2H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| D. | 甲醛溶液与足量的银氨溶液共热:HCHO+2[Ag(NH3)2]++2OH$\stackrel{△}{→}$CO32-+2NH4++2Ag↓+2NH3+H2O |
4.“类推”常用的学习方法,但有时会产生错误结论.下列类推的结论中,正确的是( )
| A. | IVA族元素氢化物沸点顺序是GeH4>SiH4>CH4,则VA族元素氢化物沸点顺序也是AsH3>PH3>NH3 | |
| B. | 常见的氢化物是分子晶体,则所有氧化物都是分子晶体 | |
| C. | 晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子 | |
| D. | 第二周期元素氢化物稳定性顺序是HF>H2O>NH3,则第三周期元素氢化物稳定性顺序也是HCl>H2S>PH3 |
8.下列试剂中,能一次鉴别出乙酸、乙醇、苯、Ba(OH)2溶液的是( )
| A. | 金属钠 | B. | 溴水 | C. | Na2CO3溶液 | D. | 紫色石蕊试液 |
18.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,4.48L Cl2溶于水所得氯水中含氯的微粒总数为0.4NA | |
| B. | 5.6g乙烯和环丁烷(C4H8)的混合气体中含的碳原子数为0.4NA | |
| C. | 常温下,pH=2的盐酸溶液中含有的H+数目为0.02NA | |
| D. | 常温下,1L 0.5mol/L的FeCl3溶液中,所含Fe3+数为0.5NA |
15.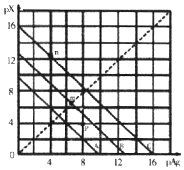 某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl、AgBr、AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX、pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是( )
某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl、AgBr、AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX、pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是( )
 某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl、AgBr、AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX、pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是( )
某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl、AgBr、AgI的Ksp依次减小.已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX、pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是( )| A. | A线是AgCl的溶解平衡曲线 | |
| B. | 坐标点p形成的溶液是AgCl的不饱和溶液 | |
| C. | m点是在水中加入足量的AgBr形成的饱和溶液 | |
| D. | n点表示由过量的KI与AgNO3反应产生AgI沉淀 |
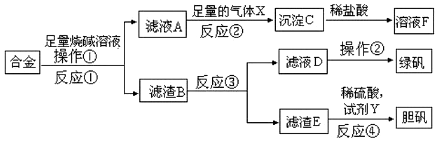
 (3)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图2:
(3)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图2: