题目内容
13.短周期主族元素X、Y、Z、W在周期表中的相对位置如表,四种元素的原子最外层电子数之和为20.下列说法正确的是( )| X | Y | Z |
| W |
| A. | W位于第三周期ⅥA族 | |
| B. | 元素最高正价:Z>Y>X | |
| C. | 简单气态氢化物稳定性:W>Y>X | |
| D. | 工业上催化氧化Y的氢化物可用于制备其含氧酸 |
分析 X、Y、Z、W均为短周期主族元素,由位置关系可知,X、Y、Z处于第二周期,W处于第三周期,设Y、W原子最外层电子数为a,则X、Z最外层电子数依次为a-1、a+1,四种元素的原子最外层电子数之和为20,则:a-1+a+a+a+1=20,解得a=5,则Y为N元素、W为P元素、X为C元素、Z为O元素,据此解答.
解答 解:X、Y、Z、W均为短周期主族元素,由位置关系可知,X、Y、Z处于第二周期,W处于第三周期,设Y、W原子最外层电子数为a,则X、Z最外层电子数依次为a-1、a+1,四种元素的原子最外层电子数之和为20,则:a-1+a+a+a+1=20,解得a=5,则Y为N元素、W为P元素、X为C元素、Z为O元素.
A.W为P元素,处于周期表中第三周期VA族,故A错误;
B.氧元素没有最高正化合价,故B错误;
C.非金属性P<N,故氢化物稳定性PH3<NH3,故C错误;
D.工业上将氨气催化氧化得到NO,NO与氧气反应生成二氧化氮,二氧化氮在与水反应得到硝酸,故D正确,
故选:D.
点评 本题考查位置结构性质的相互关系及应用,熟悉元素周期表结构及原子结构是解本题关键,注意把握元素周期律,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.在理论上不能用于设计原电池的化学反应是( )
| A. | H2SO4(aq)+BaCl2(aq)═BaSO4(s)+2HCl(aq)△H<0 | |
| B. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H<0 | |
| C. | 4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)△H<0 | |
| D. | 3Cu(s)+8HNO3(aq)═3Cu(NO3)2(aq)+2NO(g)+4H2O(l)△H<0 |
4.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 为了防止电池中的重金属等污染土壤和水体,应积极开发废电池回收利用技术 | |
| C. | 工业上采用电解熔融氯化铝制取金属铝 | |
| D. | 金属的腐蚀分为化学腐蚀和电化学腐蚀,但二者的本质相同 |
1.向下列液体中滴加稀硫酸,开始时生成沉淀,继续滴加稀H2SO4沉淀又溶解的是( )
| A. | Na2CO3溶液 | B. | BaCl2溶液 | C. | NaAlO2溶液 | D. | Fe(OH)3胶体 |
18.A、B、C、D、M均为中学化学常见物质,它们的转化关系如图所示(部分生成物和反应条件略去),其中A与H2O的反应在常温下进行,下列推断不正确的是( )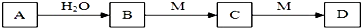
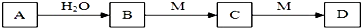
| A. | 若M为具有臭鸡蛋气味的气体,则D可能为酸式盐,且M(A)=M(C) | |
| B. | 若M为铁,则向D的溶液中通入A可能得C | |
| C. | 若C为纯碱,C转化为D的反应是CO32-+H2O+CO2═2HCO3-,则A可能为氯气 | |
| D. | 若M为可溶性铝盐,则A与水反应可能产生氢气,也可能产生氧气 |
2.中草药秦皮中含有的七叶树内酯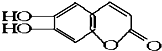 ,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )
,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )
 ,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )
,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )| A. | 3mol Br2;2mol NaOH | B. | 3mol Br2;4mol NaOH | ||
| C. | 2mol Br2;3mol NaOH | D. | 4mol Br2;4mol NaOH |
3.下列物质或离子间转化,不能一步反应完成的是( )
| A. | SiO2→H2SiO3 | B. | Al→AlO2- | C. | Na2CO3→NaOH | D. | Fe→Fe2+ |
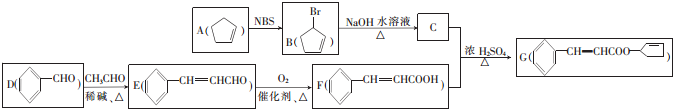
 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$ +NaBr,其反应类型为取代反应.
+NaBr,其反应类型为取代反应.