题目内容
4.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 为了防止电池中的重金属等污染土壤和水体,应积极开发废电池回收利用技术 | |
| C. | 工业上采用电解熔融氯化铝制取金属铝 | |
| D. | 金属的腐蚀分为化学腐蚀和电化学腐蚀,但二者的本质相同 |
分析 A、利用胶体具有大的表面积,有吸附作用分析;
B、废旧电池中含有汞、镉和铅等重金属元素,对人体有害;
C、氯化铝为共价化合物,熔融状态不导电;
D、金属腐蚀的本质是金属失电子被氧化的过程.
解答 解:A、明矾水解形成的Al(OH)3胶体具有较大的表面积能吸附水中悬浮物,可用于水的净化,故A正确;
B、废旧电池中含有汞、镉和铅等重金属元素,对人体有害,应积极开发废电池的综合利用技术,充分回收利用,故B正确;
C、氯化铝为共价化合物,熔融状态不导电,工业上采用电解熔融氧化铝制取金属铝,故C错误;
D、金属腐蚀的本质是金属失电子被氧化的过程,化学腐蚀和电化学腐蚀都发生氧化还原反应而导致金属腐蚀,故D正确;
故选C.
点评 本题考查较为综合,但题目难度不大,本题注意相关基础知识的积累,学习中注意金属的腐蚀等知识.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
14.下列关于化学键的说法,正确的是( )
| A. | 化合物中一定没有非极性键 | |
| B. | 单质中不可能含有离子键 | |
| C. | 金属元素与非金属元素间形成的键均是离子键 | |
| D. | CO2、CH4分子中每个原子最外层均形成了8电子结构 |
19.下列有关物质的性质和应用均正确的是( )
| A. | 酒精能使蛋白质变性,医学上使用无水酒精来杀菌消毒 | |
| B. | NH3溶于水后显碱性,在FeCl3饱和溶液中通入足量NH3可制取Fe(OH)3胶体 | |
| C. | ClO2具有强氧化性,可用于自来水的杀菌消毒,有优于氯气的高效安全性 | |
| D. | Na2CO3能与盐酸反应,广泛用于治疗胃酸过多 |
9.将m g的某种可燃物A在过量的氧气中充分燃烧,再将燃烧的产物通过足量Na2O2充分地吸收,发现固体增加的质量大于m g.则可燃物A可能是( )
| A. | 一氧化碳 | B. | 乙醇(C2H5OH) | C. | 甲酸(HCOOH) | D. | 甲醇(CH3OH) |
13.短周期主族元素X、Y、Z、W在周期表中的相对位置如表,四种元素的原子最外层电子数之和为20.下列说法正确的是( )
| X | Y | Z |
| W |
| A. | W位于第三周期ⅥA族 | |
| B. | 元素最高正价:Z>Y>X | |
| C. | 简单气态氢化物稳定性:W>Y>X | |
| D. | 工业上催化氧化Y的氢化物可用于制备其含氧酸 |


 ),丙酮(CH3COCH3)和乙醛混合物1.75g,完全燃烧后,所得气体通过P2O5吸收瓶,瓶增重1.8g,则混合物的平均相对分子质量为( )
),丙酮(CH3COCH3)和乙醛混合物1.75g,完全燃烧后,所得气体通过P2O5吸收瓶,瓶增重1.8g,则混合物的平均相对分子质量为( )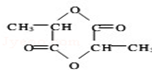 +2H2O.
+2H2O.