题目内容
1.向下列液体中滴加稀硫酸,开始时生成沉淀,继续滴加稀H2SO4沉淀又溶解的是( )| A. | Na2CO3溶液 | B. | BaCl2溶液 | C. | NaAlO2溶液 | D. | Fe(OH)3胶体 |
分析 先判断硫酸与各选项物质是否发生反应,若反应是否有白色沉淀生成,再判断白色沉淀是否溶于硫酸,据此解答.
解答 解:A、Na2CO3与H2SO4反应生成二氧化碳气体,没有沉淀生成,故A错误;
B、BaCl2与H2SO4反应:BaCl2+H2SO4=BaSO4↓+2HCl,生成BaSO4白色沉淀,不溶于硫酸,继续滴加稀硫酸,沉淀不溶解,故B错误;
C、NaAlO2与H2SO4反应:2NaAlO2+H2SO4+2H2O=2Al(OH)3↓+Na2SO4,生成Al(OH)3白色沉淀,继续滴加稀硫酸,Al(OH)3又与H2SO4反应:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O,沉淀溶解,故C正确;
D、Fe(OH)3胶体中加入硫酸溶液,开始胶体发生聚沉,当硫酸较多时会与氢氧化铁沉淀发生中和反应,沉淀又溶解,故D正确;
故选CD.
点评 本题考查物质之间的反应,注意现象是反应的体现,关键是清楚物质的性质及物质间的反应,注重基础知识的积累,题目难度不大.

练习册系列答案
相关题目
11.“封管实验”具有简易、方便、节约、绿色等优点,观察下列四幅图(夹持装置未画出),判断下列说法正确的是( )


| A. | 加热时,a上部聚集了固体NH4Cl,说明NH4Cl的热稳定性比较好 | |
| B. | 加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色的固体 | |
| C. | 加热时,c中溶液红色变深,冷却后又变浅 | |
| D. | ④左侧为e右侧为f,在惰性电极e和f附近分别滴加紫色石蕊试液,e电极附近呈红色,f电极附近呈蓝色 |
9.将m g的某种可燃物A在过量的氧气中充分燃烧,再将燃烧的产物通过足量Na2O2充分地吸收,发现固体增加的质量大于m g.则可燃物A可能是( )
| A. | 一氧化碳 | B. | 乙醇(C2H5OH) | C. | 甲酸(HCOOH) | D. | 甲醇(CH3OH) |
6.用1L1.5mol•L-1的氢氧化钠吸收标准状况下22.4LCO2,所得溶液中的CO32-和HCO3-的物质的量浓度之比为( )
| A. | 1:3 | B. | 1:2 | C. | 1:1 | D. | 3:2 |
13.短周期主族元素X、Y、Z、W在周期表中的相对位置如表,四种元素的原子最外层电子数之和为20.下列说法正确的是( )
| X | Y | Z |
| W |
| A. | W位于第三周期ⅥA族 | |
| B. | 元素最高正价:Z>Y>X | |
| C. | 简单气态氢化物稳定性:W>Y>X | |
| D. | 工业上催化氧化Y的氢化物可用于制备其含氧酸 |
 ),丙酮(CH3COCH3)和乙醛混合物1.75g,完全燃烧后,所得气体通过P2O5吸收瓶,瓶增重1.8g,则混合物的平均相对分子质量为( )
),丙酮(CH3COCH3)和乙醛混合物1.75g,完全燃烧后,所得气体通过P2O5吸收瓶,瓶增重1.8g,则混合物的平均相对分子质量为( )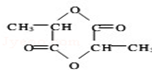 +2H2O.
+2H2O.