题目内容
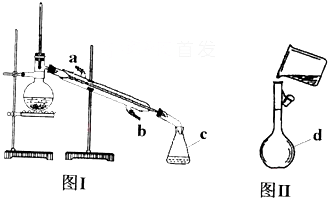
 将滴加酚酞的NaCl溶液滴在铜板上的铁柳钉处,如图所示,一段时间后发现铁柳钉的外沿处形成了棕色铁锈,下列有关说法正确的是( )
将滴加酚酞的NaCl溶液滴在铜板上的铁柳钉处,如图所示,一段时间后发现铁柳钉的外沿处形成了棕色铁锈,下列有关说法正确的是( )| A、液滴下的铜板是负极 |
| B、一段时间后会看到液滴中出现红色 |
| C、液滴中的Na+由铜板向铁柳钉迁移 |
| D、液滴下的Fe因发生还原反应而被腐蚀,此过程中还涉及到反应:4Fe(OH)2+2H20+O2=4Fe(OH)3 |
考点:原电池和电解池的工作原理
专题:
分析:铁板在氯化钠溶液中发生吸氧腐蚀,属于原电池,Fe作原电池负极,Cu作原电池正极,负极上Fe失电子,正极上氧气得电子生成氢氧根离子,据此分析.
解答:
解:A.Cu、Fe构成原电池时,活泼性强的Fe作负极,故A错误;
B.正极上氧气得电子生成氢氧根离子,所以加酚酞会变红色,故B正确;
C.溶液中阳离子向正极移动,则液滴中的Na+由铁柳钉向铜板迁移,故C错误;
D.负极上发生的电极反应式为:Fe-2e-=Fe2+,正极上的电极反应式为:O2+2H2O+4e-=4OH-,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定,容易被空气中的氧气氧化生成氢氧化铁,反应方程式为:4Fe(OH)2+2H2O+O2=4Fe(OH)3,故D正确.
故选BD.
B.正极上氧气得电子生成氢氧根离子,所以加酚酞会变红色,故B正确;
C.溶液中阳离子向正极移动,则液滴中的Na+由铁柳钉向铜板迁移,故C错误;
D.负极上发生的电极反应式为:Fe-2e-=Fe2+,正极上的电极反应式为:O2+2H2O+4e-=4OH-,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定,容易被空气中的氧气氧化生成氢氧化铁,反应方程式为:4Fe(OH)2+2H2O+O2=4Fe(OH)3,故D正确.
故选BD.
点评:本题以原电池原理为载体考查了金属的腐蚀,难度不大,明确钢铁发生析氢腐蚀和吸氧腐蚀的条件是解本题的关键,注意钢铁的吸氧腐蚀中还含有氢氧化亚铁生成氢氧化铁的反应.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、已知稀盐酸和稀NaOH溶液反应生成1molH2O时放出57.3kJ的热量,则稀硫酸和氢氧化钡溶液反应生成1molH2O时也放出57.3kJ的热量 | ||
B、C(石墨)+
| ||
| C、同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 | ||
| D、已知:①S(g)+O2(g)=SO2(g)△H=akJ.mol-1②S(s)+O2(g)=SO2(g)△H=bkJ.mol-1,则a<b |
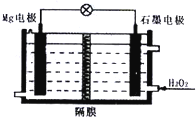 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图,该电池工作时,下列说法不正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图,该电池工作时,下列说法不正确的是( )| A、Mg电极是该电池的负极 |
| B、H2O2在石墨电极上的反应式:H2O2+2e-═2OH- |
| C、若隔膜为阳离子交换膜,则正极区有白色沉淀 |
| D、溶液中Cl-向石墨电极移动 |
X、Y、Z、R和W代表原子序数依次增大的5种短周期元素,X与Z、Y与W同主族,Y是地壳中含量最多的元素,W元素与X元素可以形成18电子的分子,R元素的简单例子是同周期元素中半径最小的,下列说法正确的是( )
| A、含R元素的盐溶液可能显酸性,也可能显碱性 |
| B、Y分别与X和Z形成化合物,这些化合物的晶体类型相同 |
| C、Y元素氢化物的沸点比W元素氢化物的沸点低 |
| D、原子半径从小到大:X<Y<R<W |
下列说法中正确的是( )
| A、焓变是指1 mol物质参加反应时的能量变化 |
| B、反应放热时,△H>0;反应吸热时,△H<0 |
| C、在一个确定的化学反应关系中,反应物的总焓与生成物的总焓一定不同 |
| D、在一个确定的化学反应关系中,反应物的总焓总是高于生成物的总焓 |
下列物质性质的变化规律,与共价键键能大小有关的是( )
| A、F2、Cl2、Br2、I2的熔点、沸点逐渐升高 |
| B、HF、HCl、HBr、HI的热稳定性依次减弱 |
| C、H2O熔沸点高于H2S.HF熔沸点高于HCl |
| D、NaF、NaCl、NaBr、Nal的熔点依次降低 |