题目内容
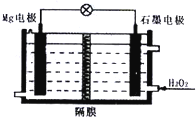 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图,该电池工作时,下列说法不正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图,该电池工作时,下列说法不正确的是( )| A、Mg电极是该电池的负极 |
| B、H2O2在石墨电极上的反应式:H2O2+2e-═2OH- |
| C、若隔膜为阳离子交换膜,则正极区有白色沉淀 |
| D、溶液中Cl-向石墨电极移动 |
考点:原电池和电解池的工作原理
专题:
分析:该装置中Mg易失电子作负极,电极反应式为Mg-2e-=Mg2+,H2O2具有氧化性,应为原电池的正极,被还原,电极反应式为H2O2+2e-═2OH-,据此分析解答.
解答:
解:A.Mg易失电子发生氧化反应而作负极,故A正确;
B.H2O2在石墨电极上得电子发生还原反应生成氢氧根离子,其电极反应式:H2O2+2e-═2OH-,故B正确;
C.若隔膜为阳离子交换膜,则镁离子向正极移动与氢氧根离子结合生成氢氧化镁白色沉淀,故C正确;
D.放电时,氯离子向负极移动,即向Mg电极移动,故D错误;
故选D.
B.H2O2在石墨电极上得电子发生还原反应生成氢氧根离子,其电极反应式:H2O2+2e-═2OH-,故B正确;
C.若隔膜为阳离子交换膜,则镁离子向正极移动与氢氧根离子结合生成氢氧化镁白色沉淀,故C正确;
D.放电时,氯离子向负极移动,即向Mg电极移动,故D错误;
故选D.
点评:本题考查了原电池原理,由Mg、双氧水的性质确定正负极,会正确书写电极反应式,知道离子移动方向,题目难度不大.

练习册系列答案
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去.下列说法不正确的是( )
A、电路中每转移12 mol电子,最多有 2 mol Cr2O
| ||
| B、阳极反应为Fe-2e-═Fe2+ | ||
| C、电解过程中溶液pH增大 | ||
| D、电解过程中有Fe(OH)3沉淀生成 |
在一定温度下,2L密闭容器内,反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
该反应达到平衡状态的时间是( )
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| N(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
| A、3 min |
| B、1 min |
| C、2 min |
| D、0 min |
下列有关金属冶炼的方法叙述正确的是( )
| A、电解氯化镁水溶液制备金属镁 |
| B、利用铝热反应制备金属铝 |
| C、加热分解Fe2O3的方法制备金属铁 |
| D、用火法或湿法均可制备金属铜 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、能使甲基橙试液显红色的溶液:Na+、NH4+、Fe2+、NO3- |
| B、含Fe3+的溶液:NH4+、K+、SCN-、Cl- |
| C、由水电离出来的c(H+)=1×10-13mol.L-1的溶液中:K+、CH3COO-、Cl-、NO3- |
| D、常温下,KW/C(H+)=0.01mol.L-1的溶液:K+、Cl-、CO32-、Na+ |
 将滴加酚酞的NaCl溶液滴在铜板上的铁柳钉处,如图所示,一段时间后发现铁柳钉的外沿处形成了棕色铁锈,下列有关说法正确的是( )
将滴加酚酞的NaCl溶液滴在铜板上的铁柳钉处,如图所示,一段时间后发现铁柳钉的外沿处形成了棕色铁锈,下列有关说法正确的是( )| A、液滴下的铜板是负极 |
| B、一段时间后会看到液滴中出现红色 |
| C、液滴中的Na+由铜板向铁柳钉迁移 |
| D、液滴下的Fe因发生还原反应而被腐蚀,此过程中还涉及到反应:4Fe(OH)2+2H20+O2=4Fe(OH)3 |
反应①与①分别是从海藻灰和碘酸钠中提取碘的主要反应,下列有关说法正确的是( )
①2Nal+MnO2+3H2S04=2NaHS04+MnS04+2H20+I2
②2NalO3+5NaHSO3=2Na2S04+3NaHSO4+H2O+l2.
①2Nal+MnO2+3H2S04=2NaHS04+MnS04+2H20+I2
②2NalO3+5NaHSO3=2Na2S04+3NaHSO4+H2O+l2.
| A、随着反应的进行,反应①与②的溶液酸性均增强 |
| B、两个反应中生成等量的I2时转移的电子数相等 |
| C、I2在反应①中是氧化产物,在反应②中是还原产物 |
| D、NaIO3在化学反应中只能作氧化剂,不能作还原剂 |