题目内容
图Ⅰ和图Ⅱ是两个实验的操作图,根据回答问题:
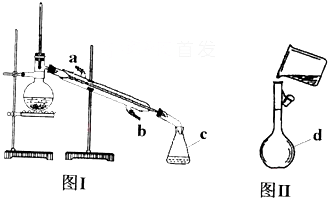
(1)写出下列仪器的名称:c ;d
(2)图Ⅰ中还缺少的玻璃仪器是(填名称)
(3)图Ⅰ在实验过程中,冷凝水由 (填a或b)流入, (填a或b)流出
(4)图Ⅱ操作中的错误是 .

(1)写出下列仪器的名称:c
(2)图Ⅰ中还缺少的玻璃仪器是(填名称)
(3)图Ⅰ在实验过程中,冷凝水由
(4)图Ⅱ操作中的错误是
考点:蒸馏与分馏
专题:化学实验基本操作
分析:(1)依据实验室常见仪器回答;
(2)依据蒸馏操作所需仪器回答;
(3)依据蒸馏操作冷凝水的流动方向回答;
(4)依据一定物质的量浓度溶液的配制方法回答.
(2)依据蒸馏操作所需仪器回答;
(3)依据蒸馏操作冷凝水的流动方向回答;
(4)依据一定物质的量浓度溶液的配制方法回答.
解答:
解:(1)仪器c为锥形瓶,d为容量瓶,故答案为:锥形瓶、容量瓶;
(2)蒸馏需要加热装置,故缺少酒精灯,故答案为:酒精灯;
(3)冷凝水应下进上出,故b流入,a流出,故答案为b;a;
(4)往容量瓶中转移液体,为防止液体外撒,应用玻璃棒引流,故错误为:未用玻璃棒引流,故答案为:未用玻璃棒引流.
(2)蒸馏需要加热装置,故缺少酒精灯,故答案为:酒精灯;
(3)冷凝水应下进上出,故b流入,a流出,故答案为b;a;
(4)往容量瓶中转移液体,为防止液体外撒,应用玻璃棒引流,故错误为:未用玻璃棒引流,故答案为:未用玻璃棒引流.
点评:本题主要考查的是实验室常见的仪器的识别、基本实验操作所需仪器以及操作注意事项,题目比较简单.

练习册系列答案
相关题目
下列实验方案正确且能达到相应实验预期目的且安全的是( )
A、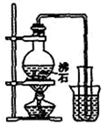 制取少量蒸馏水 |
B、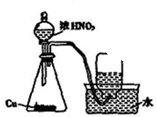 用铜和浓硝酸制取少量NO3 |
C、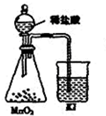 比较MnO2、Cl2、I2的氧化性 |
D、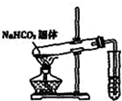 探究NaHCO3的热稳定性 |
下列说法正确的是( )
| A、工业制漂白粉是将氯气通入石灰水中制备 |
| B、海水中提取溴的方法是在经处理得到的含溴单质的水中鼓入热空气或水蒸气使溴单质挥发出来 |
| C、硫粉在过量的纯氧中燃烧可以生成三氧化硫 |
| D、少量二氧化碳通入氯化钙溶液中能生成白色沉淀 |
下列各组数据中,其比值为2:1的是( )
| A、常温下,氨水与(NH4)2SO4溶液混合后pH=7的溶液中,c(NH4+):c(SO42-) |
| B、相同温度下,1 mol.L-1醋酸与0.5mol.L-1醋酸中c(H+)之比 |
| C、用同浓度盐酸中和相同体积pH均为12的Ba(OH)2和KOH,所需盐酸的体积之比 |
| D、pH=2的H2SO4溶液与pH=2的CH3COOH溶液中,c(CH3COOH):c(H2SO4) |
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去.下列说法不正确的是( )
A、电路中每转移12 mol电子,最多有 2 mol Cr2O
| ||
| B、阳极反应为Fe-2e-═Fe2+ | ||
| C、电解过程中溶液pH增大 | ||
| D、电解过程中有Fe(OH)3沉淀生成 |
某混合溶液中可能含有下列离子中的若干种:NH4+、Na+、Al3+、Fe2+、AlO2-、SO42-、I-、NO3-、CO32-,已知离子浓度均为0.1mol.L-1.现取两份20mL该溶液进行如下实验:(1)第一份加入足量盐酸,产生气体在空气中变为红色,在反应后的溶液中加入BaCl2溶液,有白色沉淀产生.(2)第二份逐滴滴加NaOH浓溶液至过量,先产生沉淀不溶解,并有气体逸出.根据上述实验,以下说法错误的是( )
| A、该混合溶液汇总一定不含有Fe3+、AlO2-、Al3+、CO32- |
| B、在溶液中滴加酚酞试液后呈红色,加入BaCl2溶液,红色褪去,并产生白色沉淀 |
| C、该混合溶液中肯定含有Fe2+、NH4-、SO42-、NO3- |
| D、通过进行焰色反应可以确定是否含有I- |
化学与环境、材料、信息、能源关系密切,下列说法正确的是( )
| A、绿色化学的核心是应用化学原理对环境污染进行治理 |
| B、开发高效氢能、太阳能等新型电动汽车,以解决城市机动车尾气排放问题 |
| C、PM 2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体 |
| D、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
体积相同的甲、乙两个容器中,分别都充有等质量的量的SO2和O2,在相同温度下发生反应,并达平衡,在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为a%,则乙容器中SO2的转化率( )
| A、等于a% | B、大于a% |
| C、小于a% | D、无法判断 |
 将滴加酚酞的NaCl溶液滴在铜板上的铁柳钉处,如图所示,一段时间后发现铁柳钉的外沿处形成了棕色铁锈,下列有关说法正确的是( )
将滴加酚酞的NaCl溶液滴在铜板上的铁柳钉处,如图所示,一段时间后发现铁柳钉的外沿处形成了棕色铁锈,下列有关说法正确的是( )| A、液滴下的铜板是负极 |
| B、一段时间后会看到液滴中出现红色 |
| C、液滴中的Na+由铜板向铁柳钉迁移 |
| D、液滴下的Fe因发生还原反应而被腐蚀,此过程中还涉及到反应:4Fe(OH)2+2H20+O2=4Fe(OH)3 |