题目内容
18.下列离子方程式书写正确的是( )| A. | 过量氯气通入溴化亚铁溶液中:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 | |
| B. | 铜片与稀硝酸反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O | |
| C. | Fe2(SO4)3的酸性溶液中通入足量硫化氢Fe3++H2S=Fe2++S↓+2H+ | |
| D. | 在碳酸氢钙溶液中加入过量氢氧化钠溶液Ca2++HCO3-+OH-=CaCO3↓+H2O |
分析 A.氯气过量,亚铁离子和溴离子都完全被氯气氧化;
B.离子方程式两边总电荷不相等,违反了电荷守恒;
C.离子方程式两边正电荷不相等,违反了电荷守恒;
D.氢氧化钠过量,反应生成碳酸钠、碳酸钙沉淀和水,离子方程式的产物中还应该存在碳酸根离子.
解答 解:A.过量氯气通入溴化亚铁溶液中,反应生成氯化铁、溴单质,反应的离子方程式为:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2,故A正确;
B.铜片与稀硝酸反应生成硝酸铜、NO气态和水,正确的离子方程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,故B错误;
C.Fe2(SO4)3的酸性溶液中通入足量硫化氢,二者发生氧化还原反应,正确的离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,故C错误;
D.在碳酸氢钙溶液中加入过量氢氧化钠溶液,离子方程式按照碳酸氢钙的化学式组成书写,正确的离子方程式为:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-,故D错误;
故选A.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
8.某有机物的结构简式如图所示:下列有关该有机物的叙述正确的是( )


| A. | 该有机物的分子式为C11H14O3 | |
| B. | 该有机物可能易溶于水且具有水果香味 | |
| C. | 该有机物可能发生的化学反应类型有:水解、酯化、氧化、取代 | |
| D. | 1mol该有机物在Ni作催化剂的条件下能与4molH2发生加成反应 |
9.体积相同、浓度相同的HCl溶液和CH3COOH溶液分别与足量的锌粒(假设锌粒的颗粒大小相同,质量也相同)反应,下列有关说法正确的是( )
| A. | 生成氢气是HCl溶液多 | |
| B. | 生成氢气是CH3COOH溶液多 | |
| C. | 反应速率是HCl溶液与锌反应的快 | |
| D. | 反应速率是CH3COOH溶液与锌反应的快 |
6.从海水中提取镁,正确的方法是( )
| A. | 海水$\stackrel{NaOH}{→}$Mg(OH)2$\stackrel{电解}{→}$Mg | |
| B. | 海水$\stackrel{HCl}{→}$MgCl2溶液→MgCl2晶体$\stackrel{电解}{→}$Mg | |
| C. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{灼烧}{→}$MgO$\stackrel{电解}{→}$Mg | |
| D. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{HCl}{→}$MgCl2溶液-→MgCl2晶体(熔融)$\stackrel{电解}{→}$Mg |
13.等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则下列说法正确的是( )
| A. | 第一块钠消耗的氧气多 | B. | 两块钠消耗的氧气一样多 | ||
| C. | 第二块钠的反应产物质量大 | D. | 两块钠的反应产物质量一样大 |
3.下列相关实验能达到预期目的是( )
| 相关实验 | 预期目的 | |
| A | 相同温度下,将等质量的大理石块、大理石粉末分别加入等体积、等浓度的盐酸和醋酸中,观察气泡产生的快慢 | 验证固体接触面积对化学反应速率的影响 |
| B | 可逆反应FeCl3(aq)+3KSCN(aq)?Fe(SCN)3(aq)+3KCl(aq) 建立平衡后,在其它条件不变时,加入KCl固体,观察体系颜色的变化 | 验证浓度对化学平衡的影响 |
| C | 将MgCl2溶液加热蒸干 | 由MgCl2溶液制备无水MgCl2 |
| D | 相同温度下,两支试管中装有等体积、等浓度的H2O2溶液,向其中分别加入少量FeCl3固体和少量的MnO2固体 | 验证不同催化剂对H2O2分解速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
7.关于化合物 ,下列叙述不正确的是( )
,下列叙述不正确的是( )
 ,下列叙述不正确的是( )
,下列叙述不正确的是( )| A. | 分子间不能形成氢键 | B. | 分子中既有极性键又有非极性键 | ||
| C. | 分子中有7个σ键和1个π键 | D. | 该分子在水中的溶解度大于2-丁烯 |
8.下列有机反应方程式书写正确且属于取代反应的是( )
| A. | CH2=CH2+Br2→CH2BrCH2Br | B. | 2CH3CH3+Cl2$\stackrel{光照}{→}$2CH3CH2Cl+H2 | ||
| C. | CH3CH2OH+Na→CH3CH2ONa+H2↑ | D. | 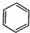 +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$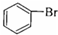 +HBr +HBr |