题目内容
20.若用NaCl固体配制100mL 1.00mol/L 的NaCl溶液.(1)所需NaCl的质量为5.9g;
(2)配制溶液用到的玻璃仪器的仪器是100 mL容量瓶、玻璃棒、胶头滴管、量筒
(3)正确的操作步骤顺序edagfbc(填写字母)
a.向小烧杯中加入适量的蒸馏水,用玻璃棒慢慢搅动,并冷却至室温;
b.盖好容量瓶瓶塞,反复颠倒、摇匀;
c.将配置好的溶液倒入指定容器中,贴好标签;
d.用天平称量NaCl固体并倒入小烧杯中;
e.计算所需的NaCl固体的质量;
f.用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转移到容量瓶中;向容量瓶中加水至离刻度线1-2cm处,改用胶头滴管逐滴滴加蒸馏水,直至凹液面与刻度相切;
g.将烧杯中的溶液沿玻璃棒转移到100mL容量瓶中.
(4)在配制过程中,如果没有洗涤烧杯和玻璃棒,其他操作都正确,那么所配溶液的实际浓度将会小于(填“大于”、“小于”或“等于”) 1.00mol/L.
分析 (1)依据m=CVM计算需要氯化钠的质量;
(2)依据配制一定物质的量浓度溶液一般步骤选择需要仪器;
(3)依据配制一定物质的量浓度溶液一般步骤排序;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)若用NaCl固体配制100mL 1.00mol/L 的NaCl溶液,需要氯化钠质量m=0.1L×1.00mol/L×58.5g/mol=5.9g;
故答案为:5.9;
(2)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、移液、洗涤、定容、摇匀等,用到的仪器:托盘天平、药匙、烧杯、100 mL容量瓶、玻璃棒、胶头滴管;用到的玻璃仪器的仪器是100 mL容量瓶、玻璃棒、胶头滴管;
故答案为:100 mL容量瓶、玻璃棒、胶头滴管;
(3)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶、贴标签,所以正确的顺序为:dagfbc;
故答案为:edagfbc;
(4)在配制过程中,如果没有洗涤烧杯和玻璃棒,导致溶质部分损耗,溶质的物质的量偏小,溶液浓度偏小;
故答案为:小于.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意依据C=$\frac{n}{V}$进行误差分析的方法和技巧.

练习册系列答案
相关题目
17.将铜和碳的混合物在空气中充分灼烧,混合物的质量在冷却后没有变化,则原混合物中铜和碳的质量比为( )
| A. | 1:1 | B. | 1:4 | C. | 4:1 | D. | 无法确定 |
18.下列关于原子结构及微粒间的数量关系的说法错误的是( )
| A. | 同种元素的原子均有相同的质子数和中子数 | |
| B. | 微粒Na+、Mg2+、O2-具有相同的电子层结构 | |
| C. | 短周期第ⅣA与ⅥIA族元素的原子间构成的分子,均满足原子最外层8电子结构 | |
| D. | ${\;}_{20}^{48}$Ca2+的中子数比核外电子数多10 |
8.某有机物的结构简式如图所示:下列有关该有机物的叙述正确的是( )


| A. | 该有机物的分子式为C11H14O3 | |
| B. | 该有机物可能易溶于水且具有水果香味 | |
| C. | 该有机物可能发生的化学反应类型有:水解、酯化、氧化、取代 | |
| D. | 1mol该有机物在Ni作催化剂的条件下能与4molH2发生加成反应 |
15.某种解热镇痛药的结构简式如图所示,当它完全水解时,不可能得到的产物是( )
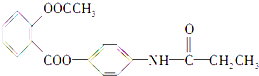
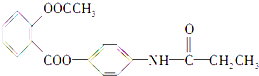
| A. | CH3CH2COOH | B. | CH3COOH | C. | CH3OH | D. | 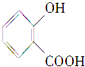 |
9.体积相同、浓度相同的HCl溶液和CH3COOH溶液分别与足量的锌粒(假设锌粒的颗粒大小相同,质量也相同)反应,下列有关说法正确的是( )
| A. | 生成氢气是HCl溶液多 | |
| B. | 生成氢气是CH3COOH溶液多 | |
| C. | 反应速率是HCl溶液与锌反应的快 | |
| D. | 反应速率是CH3COOH溶液与锌反应的快 |