题目内容
9.一定温度下,可逆反应3X(g)+Y(g)?2Z(g)达到化学平衡状态的标志是( )| A. | 单位时间内生成3n mol X,同时消耗n mol Y | |
| B. | X的生成速率与Z的消耗速率相等 | |
| C. | X、Y、Z的浓度相等 | |
| D. | X、Y、Z的物质的量之比为3:1:2 |
分析 可逆反应3X(g)+Y(g)?2Z(g)为气体体积缩小的反应,当达到化学平衡状态时,正逆反应速率相等,反应物的浓度、百分含量不再发生改变,由此衍生的一些物理性也不再变化,以此进行解答.
解答 解:A.单位时间内生成3nmolX,同时消耗nmolY,说明正逆反应速率相等,达到平衡状态,故A正确;
B.X的生成速率与Z的消耗速率相等,表示的都是逆反应,且不满足计量数关系,无法判断是否达到平衡状态,故B错误;
C.X、Y、Z的浓度相等,无法判断各组分的浓度是否不再变化,则无法判断平衡状态,故C错误;
D.X、Y、Z的物质的量之比为3:1:2,无法判断各组分的物质的量是否不变,则无法判断平衡状态,故D错误;
故选A.
点评 本题考查化学平衡状态的判断,题目难度不大,明确化学平衡状态的特征为解答关键,C、D为易错点,注意只有变量不再变化才达到平衡状态,不能根据浓度是否相等、物质的量之比判断平衡状态.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
19. 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A. | 原子半径:rW>rZ>rY>rX | |
| B. | 含Y元素的盐溶液有的显酸性,有的显碱性 | |
| C. | 最简单气态氢化物的热稳定性:Z>W | |
| D. | 元素X的气态氢化物能与其最高价氧化物对应水化物反应 |
20.关于下列各装置图的叙述中,不正确的是( )


| A. | 用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 | |
| B. | 用装置①进行电镀,镀件接在b极上 | |
| C. | 装置①的a极为阴极 | |
| D. | 装置②的总反应是:Cu+2Fe3+═Cu2++2Fe2+ |
14.下列电离方程式正确的是( )
| A. | CuSO4═Cu+2+SO4-2 | B. | NH4NO3═NH4++NO3- | ||
| C. | Na2CO3═Na2++CO32- | D. | KClO3═K++Cl-+3O2- |
8.下列分子或离子之间互为等电子体的是( )
| A. | CH4和H3O+ | B. | NO3- 和SO3 | C. | O3和CO2 | D. | N2和C22- |
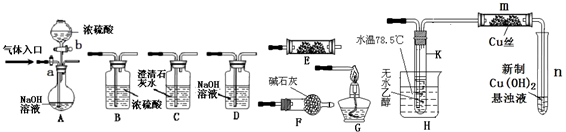
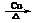 2CH3CHO+2H2O
2CH3CHO+2H2O