题目内容
8.下列分子或离子之间互为等电子体的是( )| A. | CH4和H3O+ | B. | NO3- 和SO3 | C. | O3和CO2 | D. | N2和C22- |
分析 先根据具有相同价电子数和相同原子数的分子或离子是等电子体,然后判断电子的数目来解答.
解答 解:A.CH4含有5个原子,H3O+含有4个原子,不是等电子体,故A错误;
B.NO3-的价电子数为5+6×3+1=24,SO3的价电子数为6×4=24,含有相同原子数4,为等电子体,故B正确;
C.O3的价电子数为6×3=18,CO2的价电子数为4+6×2=16,不是等电子体,故C错误;
D.N2的价电子数为5×2=10,C22-的价电子数为4×2+2=10,含有相同原子数2,为等电子体,故D正确;
故选BD.
点评 本题主要考查了等电子体,解答本题的关键是要充分理解等电子体的本质特征,只有这样才能对问题做出正确的判断,题目难度不大.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
9.一定温度下,可逆反应3X(g)+Y(g)?2Z(g)达到化学平衡状态的标志是( )
| A. | 单位时间内生成3n mol X,同时消耗n mol Y | |
| B. | X的生成速率与Z的消耗速率相等 | |
| C. | X、Y、Z的浓度相等 | |
| D. | X、Y、Z的物质的量之比为3:1:2 |
10.X、Y、Z三者均为短周期元素,已知X元素有一种同位素不含中子,Y元素原子的最外层电子数是次外层电子数的2倍,Z元素原子的最外层电子数是次外层电子数的3倍.下列化学式①XYZ3②X2YZ2③X2YZ3④X2Y2Z2⑤X2Y2Z4⑥X4Y2Z2中,并非都存在的一组分子是( )
| A. | ①② | B. | ④⑥ | C. | ③⑤ | D. | ②④ |
3.下列措施或事实不能用勒沙特列原理解释的是( )
| A. | 新制的氯水在光照下颜色变浅 | |
| B. | NO2和N2O4平衡混合气缩小体积加压后颜色变深 | |
| C. | 硫酸工业上SO2氧化成SO3,宜采用空气过量 | |
| D. | 煅烧硫铁矿利于SO2的生成 |
17. 取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略)
取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略)
请回答下列问题:
(1)实验1、2研究的是温度对H2O2分解速率的影响.
(2)实验2、3的目的是不同催化剂对过氧化氢分解速率的影响.
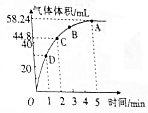
(3)加入0.1mol MnO2粉末于50mL过氧化氢溶液(密度为1.1g•mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.
①A、B、C、D四点的化学反应速率快慢的顺序为D>C>B>A.
②过氧化氢的初始物质的量浓度为0.104 mol•L-1.
③反应进行到2min时过氧化氢的质量分数为0.074%.
 取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略)
取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略) | 序号 | 条件 | 现象和结论 | |
| 温度/℃ | 催化剂 | ||
| 1 | 40 | FeCl3溶液 | |
| 2 | 20 | FeCl3溶液 | |
| 3 | 20 | MnO2 | |
(1)实验1、2研究的是温度对H2O2分解速率的影响.
(2)实验2、3的目的是不同催化剂对过氧化氢分解速率的影响.
(3)加入0.1mol MnO2粉末于50mL过氧化氢溶液(密度为1.1g•mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.
①A、B、C、D四点的化学反应速率快慢的顺序为D>C>B>A.
②过氧化氢的初始物质的量浓度为0.104 mol•L-1.
③反应进行到2min时过氧化氢的质量分数为0.074%.
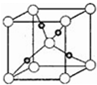 ④在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为;1mol尿素分子中,σ 键的数目为7NA.
④在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为;1mol尿素分子中,σ 键的数目为7NA.
 .
. 、
、 、
、 (其中三种).
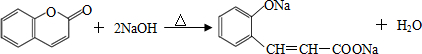
(其中三种). 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 .
. 肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.
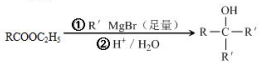
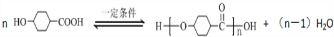 .
. .
.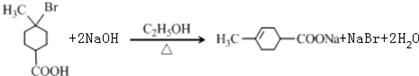 .
.