题目内容
下列物质都具有漂白性,其中漂白原理与其他三种不同的是( )
| A、双氧水 | B、二氧化硫 |
| C、氯水 | D、臭氧 |
考点:二氧化硫的化学性质
专题:氧族元素
分析:H2O2、O3、氯水中HClO均具有强氧化性,能使有色物质褪色,而SO2不具有强氧化性,它与有色物质化合生成无色物质,以此来解答.
解答:
解:A.因H2O2具有强氧化性,则能使有色物质褪色;
B.SO2不具有强氧化性,它与有色物质化合生成无色物质;
C.因氯水中HClO具有强氧化性,则能使有色物质褪色;
D.因O3具有强氧化性,则能使有色物质褪色;
显然只有B的漂白原理与其他几种不同,
故选B.
B.SO2不具有强氧化性,它与有色物质化合生成无色物质;
C.因氯水中HClO具有强氧化性,则能使有色物质褪色;
D.因O3具有强氧化性,则能使有色物质褪色;
显然只有B的漂白原理与其他几种不同,
故选B.
点评:本题考查二氧化硫的性质,为高频考点,注意其漂白原理是利用化合反应生成无色物质,属于暂时性的漂白,题目难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
将5.1g镁铝合金,投入500mL 2.0mol?L-1盐酸中,金属完全溶解,再加入4.0mol?L-1的NaOH溶液,若要生成的沉淀最多,则加入NaOH溶液的体积是( )
| A、200mL |
| B、425mL |
| C、250mL |
| D、560mL |
下列物质中互为同分异构体的是( )
| A、CH3CH2CH2CH3 |
B、 |
C、 |
| D、CH3CH2CH2CH2Cl |
在下列反应中,硝酸既表现氧化性又表现酸性的是( )
| A、C和浓HNO3 |
| B、Al(OH)3和HNO3 |
| C、H2S和HNO3 |
| D、Fe3O4和HNO3 |
下列物质的说法正确的是( )
| A、芳香烃可以来自于煤干馏产品中的煤焦油 |
| B、聚氯乙烯可用于制作食品包装袋 |
| C、镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀 |
| D、在铁的吸氧腐蚀中,负极是炭,电极反应为2H2O+O2+4e-=4OH- |
在一种一元碱ROH的溶液中,加入一种一元酸HA溶液,当反应后溶液呈现中性,下列判断中一定正确的是( )
| A、反应后溶液中C(A-)=C(R+) |
| B、加入的酸与碱的物质的量相等 |
| C、生成的盐RA不能发生水解 |
| D、加入的一元酸HA过量 |
下列化学用语正确的是( )
A、H2S的电子式: |
B、钙原子结构示意图: |
C、Na2O2的电子式: |
| D、铁离子:Fe2+ |
绿色化学对于化学反应提出了“原子经济性”的要求.理想的原子经济性反应是原料中的原子全部转化为产物,不产生副产品,实现零排放.下列几种生产乙苯的方法中,原子经济性最好的是( )
A、 +C2H5Cl→ +C2H5Cl→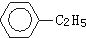 +HCl +HCl |
B、 +C2H5OH→ +C2H5OH→ +H2O +H2O |
C、 +CH2═CH2→ +CH2═CH2→ |
D、 +CH3CH3→ +CH3CH3→ +HCl +HCl |