题目内容
下列化学用语正确的是( )
A、H2S的电子式: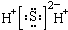 |
B、钙原子结构示意图: |
C、Na2O2的电子式: |
| D、铁离子:Fe2+ |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.硫化氢为共价化合物,硫化氢分子中不存在阴阳离子,其电子式不能标出电荷;
B.钙原子最外层为2个电子,原子结构示意图中,最外层不能超过8个电子;
C.过氧化钠为离子化合物,钠离子直接用离子符号表示,过氧根离子需要标出电荷及原子的最外层电子;
D.铁离子带有3个单位正电荷,Fe2+为亚铁离子.
B.钙原子最外层为2个电子,原子结构示意图中,最外层不能超过8个电子;
C.过氧化钠为离子化合物,钠离子直接用离子符号表示,过氧根离子需要标出电荷及原子的最外层电子;
D.铁离子带有3个单位正电荷,Fe2+为亚铁离子.
解答:
解:A.硫化氢中不存在阴阳离子,硫化氢中存在2个S-H共用电子对,硫化氢正确的电子式为: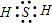 ,故A错误;
,故A错误;
B.钙原子的核电荷数=核外电子总数=20,最外层为2个电子,钙原子正确的结构示意图为: ,故B错误;
,故B错误;
C.过氧化钠属于离子化合物,电子式中阴阳离子需要标出所带电荷,阴离子还需要标出原子的最外层电子,过氧化钠的电子式为: ,故C正确;
,故C正确;
D.Fe2+为亚铁离子,铁离子带有3个单位正电荷,铁离子应该表示为:Fe3+,故D错误;
故选C.
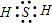 ,故A错误;
,故A错误;B.钙原子的核电荷数=核外电子总数=20,最外层为2个电子,钙原子正确的结构示意图为:
 ,故B错误;
,故B错误;C.过氧化钠属于离子化合物,电子式中阴阳离子需要标出所带电荷,阴离子还需要标出原子的最外层电子,过氧化钠的电子式为:
 ,故C正确;
,故C正确;D.Fe2+为亚铁离子,铁离子带有3个单位正电荷,铁离子应该表示为:Fe3+,故D错误;
故选C.
点评:本题考查了电子式、原子结构示意图、结构式、离子符号的表示方法判断,题目难度中等,注意掌握常见的化学用语的概念及正确的表示方法,明确原子结构示意图与离子结构示意图、离子化合物与共价化合物的电子式的区别.

练习册系列答案
相关题目
常温下,0.1mol?L-1 CH3COONa溶液中,微粒浓度间关系正确的是( )
| A、c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| B、c(OH-)=c(H+)+c(CH3COOH) |
| C、c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| D、c(CH3COOH)+c(CH3COO-)=c(Na+)+c(H+) |
能正确表示下列反应的离子方程式的是( )
| A、氧化亚铁与稀硝酸反应:FeO+2H+═Fe2++H2O |
| B、氢氧化钡与稀硫酸反应:Ba2++SO42-﹦BaSO4↓ |
| C、铜与浓硝酸反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| D、氯化铵溶液加入氢氧化钠溶液:NH4++OH-=NH3↑+H2O |
下列物质都具有漂白性,其中漂白原理与其他三种不同的是( )
| A、双氧水 | B、二氧化硫 |
| C、氯水 | D、臭氧 |
设NA为阿伏加德罗常数,下列叙述中错误的是( )
| A、在标准状况下,22.4L空气中约有NA个气体分子 |
| B、在含4mol Si-O键的石英晶体中,氧原子的数目为2NA |
| C、28g乙烯和28g丙烯中均含有6NA对共用电子对 |
| D、含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2:3 |
下列离子方程式正确的是( )
A、用石墨作电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| B、硫酸镁溶液与氢氧化钡溶液混合:SO42-+Ba2+═BaSO4↓ | ||||
| C、Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | ||||
| D、AlCl3溶液中加入过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
下列元素中,金属性最强的是( )
| A、K | B、Al | C、He | D、S |
