题目内容
下列物质的说法正确的是( )
| A、芳香烃可以来自于煤干馏产品中的煤焦油 |
| B、聚氯乙烯可用于制作食品包装袋 |
| C、镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀 |
| D、在铁的吸氧腐蚀中,负极是炭,电极反应为2H2O+O2+4e-=4OH- |
考点:金属的电化学腐蚀与防护,有机化学反应的综合应用
专题:电化学专题
分析:A.煤干馏能得到煤焦油,煤焦油中含有芳香烃;
B.聚氯乙烯不能包装食品;
C.作原电池负极的金属加速被腐蚀、作原电池正极的金属被保护;
D.铁的吸氧腐蚀中,铁作负极、C作正极,正极上氧气得电子生成氢氧根离子,负极上铁失电子生成亚铁离子.
B.聚氯乙烯不能包装食品;
C.作原电池负极的金属加速被腐蚀、作原电池正极的金属被保护;
D.铁的吸氧腐蚀中,铁作负极、C作正极,正极上氧气得电子生成氢氧根离子,负极上铁失电子生成亚铁离子.
解答:
解:A.煤干馏能得到煤焦油,煤焦油中含有芳香烃,所以芳香烃可以来自于煤干馏产品中的煤焦油,故A正确;
B.聚氯乙烯(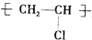 )有毒,不能用于制作食品保鲜袋,故B错误;
)有毒,不能用于制作食品保鲜袋,故B错误;
C.作原电池负极的金属加速被腐蚀、作原电池正极的金属被保护,镀层破损后,白铁(镀锌的铁)中铁作正极被保护,马口铁(镀锡的铁)中铁作负极加速被腐蚀,所以马口铁(镀锡的铁)更易腐蚀,故C错误;
D.铁的吸氧腐蚀中,铁作负极、C作正极,正极上氧气得电子生成氢氧根离子,负极上铁失电子生成亚铁离子,负极电极反应为Fe-2e-=Fe2+、正极反应为2H2O+O2+4e-=4OH-,故D错误;
故选A.
B.聚氯乙烯(
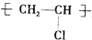 )有毒,不能用于制作食品保鲜袋,故B错误;
)有毒,不能用于制作食品保鲜袋,故B错误;C.作原电池负极的金属加速被腐蚀、作原电池正极的金属被保护,镀层破损后,白铁(镀锌的铁)中铁作正极被保护,马口铁(镀锡的铁)中铁作负极加速被腐蚀,所以马口铁(镀锡的铁)更易腐蚀,故C错误;
D.铁的吸氧腐蚀中,铁作负极、C作正极,正极上氧气得电子生成氢氧根离子,负极上铁失电子生成亚铁离子,负极电极反应为Fe-2e-=Fe2+、正极反应为2H2O+O2+4e-=4OH-,故D错误;
故选A.
点评:本题考查有机物的性质、原电池原理,根据原电池中各个电极上发生的反应、得失电子即可解答,注意聚氯乙烯不能作食品包装袋,会运用化学知识解释生活现象,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
将CO2通入下列溶液中,一定不会产生沉淀的是( )
| A、澄清的石灰水 |
| B、氯化钡溶液 |
| C、饱和碳酸钠溶液 |
| D、偏铝酸钠溶液 |
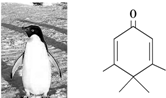 如右图所示的分子酷似企鹅,化学家将该分子以企鹅来取名为Penguinone.下列有关说法错误的是( )
如右图所示的分子酷似企鹅,化学家将该分子以企鹅来取名为Penguinone.下列有关说法错误的是( )| A、Penguinone分子式为C10H14O |
| B、Penguinone是一种芳香族化合物 |
| C、Penguinone可以使酸性高锰酸钾溶液褪色 |
| D、Penguinone能与H2发生加成反应 |
能正确表示下列反应的离子方程式的是( )
| A、氧化亚铁与稀硝酸反应:FeO+2H+═Fe2++H2O |
| B、氢氧化钡与稀硫酸反应:Ba2++SO42-﹦BaSO4↓ |
| C、铜与浓硝酸反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| D、氯化铵溶液加入氢氧化钠溶液:NH4++OH-=NH3↑+H2O |
化学与工农业生产和人类生活密切相关.下列说法中,不正确的是( )
| A、油脂在碱性条件下水解可制得肥皂 |
| B、海轮外壳上镶入锌块,可减缓船体的腐蚀 |
| C、人体中缺碘元素会得贫血病 |
| D、研制推广甲醇燃料汽车,有利于“减排目标”的实现 |
下列物质都具有漂白性,其中漂白原理与其他三种不同的是( )
| A、双氧水 | B、二氧化硫 |
| C、氯水 | D、臭氧 |
设NA为阿伏加德罗常数,下列叙述中错误的是( )
| A、在标准状况下,22.4L空气中约有NA个气体分子 |
| B、在含4mol Si-O键的石英晶体中,氧原子的数目为2NA |
| C、28g乙烯和28g丙烯中均含有6NA对共用电子对 |
| D、含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2:3 |
下列元素中,金属性最强的是( )
| A、K | B、Al | C、He | D、S |
 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.