题目内容
钠及其重要化合物之间的转化关系如图所示:
Na2O2←Na
NaOH→Na2CO3
NaHCO3
回答下列问题:
(1)少量的金属钠应保存在 中.
(2)Na2O2的颜色为 .
(3)反应①的氧化剂是 .
(4)Na2CO3溶液与BaCl2溶液反应产生白色沉淀,其中Na2CO3参加反应的离子是 (填“Na+”或“CO32-”).
(5)反应②的化学方程式为 .
Na2O2←Na
| ①H2O |
| CO2+H2O |
| ②△ |
回答下列问题:
(1)少量的金属钠应保存在
(2)Na2O2的颜色为
(3)反应①的氧化剂是
(4)Na2CO3溶液与BaCl2溶液反应产生白色沉淀,其中Na2CO3参加反应的离子是
(5)反应②的化学方程式为
考点:钠的重要化合物
专题:元素及其化合物
分析:(1)钠性质活泼,应保存在煤油中;
(2)Na2O2的颜色为淡黄色;
(3)钠和水反应生成氢氧化钠和氢气,H元素化合价降低,Na元素化合价升高;
(4)Na2CO3溶液与BaCl2溶液反应生成碳酸钡沉淀;
(5)碳酸氢钠不稳定,加热易分解生成碳酸钠、水和二氧化碳.
(2)Na2O2的颜色为淡黄色;
(3)钠和水反应生成氢氧化钠和氢气,H元素化合价降低,Na元素化合价升高;
(4)Na2CO3溶液与BaCl2溶液反应生成碳酸钡沉淀;
(5)碳酸氢钠不稳定,加热易分解生成碳酸钠、水和二氧化碳.
解答:
解:(1)钠性质活泼,易与空气中水、氧气反应,而与煤油、石蜡油不反应,且密度不煤油、石蜡油大,应保存在煤油或石蜡油中,
故答案为:煤油或石蜡油;
(2)Na2O2的颜色为淡黄色,故答案为:淡黄色;
(3)钠和水反应生成氢氧化钠和氢气,H元素化合价降低,Na元素化合价升高,氧化剂为H2O,故答案为:H2O;
(4)Na2CO3溶液与BaCl2溶液反应生成碳酸钡沉淀,参加反应的离子为CO32-,故答案为:CO32-;
(5)碳酸氢钠不稳定,加热易分解生成碳酸钠、水和二氧化碳,反应的方程式为2NaHCO3
Na2CO3+CO2↑+H2O,
故答案为:2NaHCO3
Na2CO3+CO2↑+H2O.
故答案为:煤油或石蜡油;
(2)Na2O2的颜色为淡黄色,故答案为:淡黄色;
(3)钠和水反应生成氢氧化钠和氢气,H元素化合价降低,Na元素化合价升高,氧化剂为H2O,故答案为:H2O;
(4)Na2CO3溶液与BaCl2溶液反应生成碳酸钡沉淀,参加反应的离子为CO32-,故答案为:CO32-;
(5)碳酸氢钠不稳定,加热易分解生成碳酸钠、水和二氧化碳,反应的方程式为2NaHCO3
| ||
故答案为:2NaHCO3
| ||
点评:本题综合考查钠的化合物,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
下列物质都具有漂白性,其中漂白原理与其他三种不同的是( )
| A、双氧水 | B、二氧化硫 |
| C、氯水 | D、臭氧 |
钛被称为21世纪金属,是研制卫星、火箭、宇宙飞船及深海潜艇的重要材料.研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置模拟获得金属钙(需定期更换石墨棒),并以钙为还原剂,还原二氧化钛制备金属钛.下列叙述正确的是( )
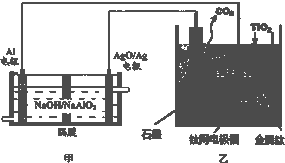

| A、甲装置工作过程中OH-向AgO/Ag极移动;乙装置工作过程中O2-向阴极移动 | ||
| B、乙装置阳极的电极反应式为C+2O2--4e-═CO2↑ | ||
C、若电解金属钛效率为η,则获取1mol Ti时消耗Al的物质的量
| ||
| D、在制备金属钛前后,整套装置中CaO的总量减少 |
下列说法不正确的是( )
| A、硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂等的原料 |
| B、将钢闸门与外加电源负极相连,可防止钢闸门被腐蚀 |
| C、CaO能与SO2反应,可作工业废气的脱硫剂 |
| D、MgO、Al2O3都是常见的耐高温材料,工业上也常用其电解冶炼对应的金属 |
 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.