题目内容
实验室需要配置0.40mol?L-1 NaCl溶液500mL.按下列操作步骤填上适当的文字,以使整个操作步骤完整.
第一步:选择仪器.完成本实验所必须的仪器有:天平(精确到0.1g)、药匙、烧杯、玻璃棒、 、 以及等质量的两片滤纸.
第二步:计算.配置该溶液需取NaCl晶体 g.
第三步:称量.
①天平调平后,应将天平的游码调至某个位置,然后称量好药品.
②称量过程中NaCl晶体应放于天平的 (填“左盘”或“右盘”).
③称量完毕,将药品倒入烧杯中.
第四步:操作名称是 ,该步实验中玻璃棒的作用是 .
第五步:转移、洗涤.在转移时应用玻棒引流,然后需要洗涤烧杯和玻棒2-3次是为了 .
第六步:定容.定容时视线应与 .
第七步:摇匀
第八步:将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配置的时间、名称及浓度.
第一步:选择仪器.完成本实验所必须的仪器有:天平(精确到0.1g)、药匙、烧杯、玻璃棒、
第二步:计算.配置该溶液需取NaCl晶体
第三步:称量.
①天平调平后,应将天平的游码调至某个位置,然后称量好药品.
②称量过程中NaCl晶体应放于天平的
③称量完毕,将药品倒入烧杯中.
第四步:操作名称是
第五步:转移、洗涤.在转移时应用玻棒引流,然后需要洗涤烧杯和玻棒2-3次是为了
第六步:定容.定容时视线应与
第七步:摇匀
第八步:将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配置的时间、名称及浓度.
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:要配置0.40mol?L-1 NaCl溶液500mL,一般操作步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到100mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加逐滴滴加的凹液面最低处于刻度线相切,然后摇匀、装瓶,据此解答.
解答:
解:(1)配置一定物质的量浓度氯化钠用到的仪器有:天平(精确到0.1g)、药匙、烧杯、玻璃棒、500ml容量瓶、胶头滴管等,
故答案为:500ml容量瓶;胶头滴管等;
(2)配置该溶液需取NaCl晶体的物质的量n=0.40mol?L-1×0.5L=0.2mol,其质量为0.2mol×58.5g/mol=11.7g,故答案为:11.7;
(3)称量固体遵循“左物右码”原则,物质应放在左盘,故答案为:左盘;
(4)称量后的固体氯化钠应放在烧杯中加入适量的蒸馏水溶解,用玻璃棒搅拌加速氯化钠的溶解速率,故答案为:溶解;搅拌加速溶解;
(5)移液后的烧杯和玻璃棒上沾有溶质氯化钠,应进行洗涤,否则氯化钠溶液流失,造成误差,故答案为:减少氯化钠流失,减小实验误差;
(6)定容时,视线应与凹液面最底处水平相切,故答案为:视线应与凹液面最底处水平相切.
故答案为:500ml容量瓶;胶头滴管等;
(2)配置该溶液需取NaCl晶体的物质的量n=0.40mol?L-1×0.5L=0.2mol,其质量为0.2mol×58.5g/mol=11.7g,故答案为:11.7;
(3)称量固体遵循“左物右码”原则,物质应放在左盘,故答案为:左盘;
(4)称量后的固体氯化钠应放在烧杯中加入适量的蒸馏水溶解,用玻璃棒搅拌加速氯化钠的溶解速率,故答案为:溶解;搅拌加速溶解;
(5)移液后的烧杯和玻璃棒上沾有溶质氯化钠,应进行洗涤,否则氯化钠溶液流失,造成误差,故答案为:减少氯化钠流失,减小实验误差;
(6)定容时,视线应与凹液面最底处水平相切,故答案为:视线应与凹液面最底处水平相切.
点评:本题考查了一定物质的量浓度溶液的配制过程、仪器,难度不大,注意实验的基本操作方法和注意事项.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
把3mol A与2.5mol B充入2L容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g).经5min达到平衡,生成1mol D,以C的浓度变化表示的反应速率是0.1mol/(L?min),则下列叙述中错误的是( )
| A、vA=0.15 mol/(L?min) |
| B、B的转化率为20% |
| C、B的平衡浓度是0.5 mol/L |
| D、x值等于2 |
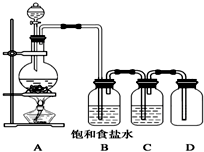 用如图装置制取并收集氯气,试回答下列问题:
用如图装置制取并收集氯气,试回答下列问题: 如图是学校实验室从化学试剂商店买回的盐酸试剂标签上的部分内容,据此,完成下列问题:
如图是学校实验室从化学试剂商店买回的盐酸试剂标签上的部分内容,据此,完成下列问题: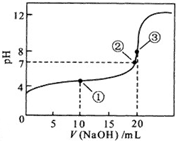 常温下,用0.10mol?L-1NaOH溶液滴定 20.00mL 0.10mol?L-1 CH3COOH溶液滴定曲线如图.
常温下,用0.10mol?L-1NaOH溶液滴定 20.00mL 0.10mol?L-1 CH3COOH溶液滴定曲线如图.