题目内容
下列叙述,正确的是( )
A、人们使用
| ||||
| B、科学家们在过渡元素中寻找催化剂 | ||||
| C、目前周期表中的所有元素都是科学家们从自然界发现的 | ||||
| D、只有主族元素同时由短周期元素和长周期元素共同构成 |
考点:元素周期律和元素周期表的综合应用,同位素及其应用
专题:元素周期律与元素周期表专题
分析:A.2H和3H都是制造氢弹的原料;
B.制耐高温合金元素、催化剂在元素周期表的过渡金属中能找到;
C.周期表中部分元素是人工合成的;
D.0族元素也是由短周期和长周期元素共同构成的.
B.制耐高温合金元素、催化剂在元素周期表的过渡金属中能找到;
C.周期表中部分元素是人工合成的;
D.0族元素也是由短周期和长周期元素共同构成的.
解答:
解:A.2H和3H都是制造氢弹的原料,不能用氕制造氢弹,故A错误;
B.制耐高温合金元素、催化剂在元素周期表的过渡金属中能找到,半导体在金属和非金属分界线处能找到,故B正确;
C.周期表中有些放射性元素是人造元素,故C错误;
D.0族和主族元素是由短周期和长周期元素共同构成的,故D错误;
故选B.
B.制耐高温合金元素、催化剂在元素周期表的过渡金属中能找到,半导体在金属和非金属分界线处能找到,故B正确;
C.周期表中有些放射性元素是人造元素,故C错误;
D.0族和主族元素是由短周期和长周期元素共同构成的,故D错误;
故选B.
点评:本题考查了元素周期表的结构和用途,根据元素在周期表中的位置确定元素的性质,再结合元素周期表结构解答,题目难度不大.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
下列叙述错误的是( )
(1)若R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R强于Q
(2)阴、阳离子通过静电吸引形成的化学键叫离子键
(3)都是由非金属元素形成的化合物只能是共价化合物.
(1)若R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R强于Q
(2)阴、阳离子通过静电吸引形成的化学键叫离子键
(3)都是由非金属元素形成的化合物只能是共价化合物.
| A、全部 | B、(1) |
| C、(2) | D、(3) |
下列叙述正确的是( )
A、S2-的结构示意图是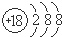 |
B、HCl的电子式为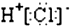 |
C、NH3的结构式为  |
| D、还原性:HCl>H2S |
用FeCl3溶液腐蚀印刷电路板上铜箔的反应是:2Fe3++Cu=2Fe2++Cu2+,该反应的还原剂是( )
| A、Fe3+ |
| B、Cu |
| C、Fe2+ |
| D、Cu2+ |
下列事实不能用勒夏特列原理解释的是( )
| A、恒温密闭容器中NO2和N2O4形成的平衡体系,减小体积,体系颜色加深 |
| B、开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| C、滴加酚酞的氨水中加入氯化铵固体后红色变浅 |
| D、工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
下列表示物质组成和结构的化学用语中,不正确的是( )
| A、甲酸的结构简式:HO-CHO |
B、一氟甲烷电子式: |
| C、聚丙烯的最简式:CH2 |
| D、次氯酸的结构式:H-O-Cl |
常温下,在pH=12的某碱溶液中,由水电离出的c(OH-)为( )
| A、1.0×10-7 mol/L |
| B、1.0×10-6 mol/L |
| C、1.0×10-3 mol/L |
| D、1.0×10-12 mol/L |
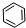 、④HCHO其中碳原子采取sp2杂化的分子有
、④HCHO其中碳原子采取sp2杂化的分子有