题目内容
下列叙述错误的是( )
(1)若R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R强于Q
(2)阴、阳离子通过静电吸引形成的化学键叫离子键
(3)都是由非金属元素形成的化合物只能是共价化合物.
(1)若R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R强于Q
(2)阴、阳离子通过静电吸引形成的化学键叫离子键
(3)都是由非金属元素形成的化合物只能是共价化合物.
| A、全部 | B、(1) |
| C、(2) | D、(3) |
考点:元素周期律的作用,化学键
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:(1)从酸性角度比较非金属性强弱,应为最高价氧化物对应的水化物的酸性;
(2)离子键既存在静电吸引又存在静电排斥;
(3)都是由非金属元素形成的化合物可能为离子化合物.
(2)离子键既存在静电吸引又存在静电排斥;
(3)都是由非金属元素形成的化合物可能为离子化合物.
解答:
解:(1)如不是最高价氧化物对应的水化物,则不能根据酸性强弱比较非金属性强弱,故(1)错误;
(2)离子键为阴阳离子之间的静电作用,既存在静电吸引又存在静电排斥,故(2)错误;
(3)都是由非金属元素形成的化合物可能为离子化合物,如铵盐等,故(3)错误,
故选A.
(2)离子键为阴阳离子之间的静电作用,既存在静电吸引又存在静电排斥,故(2)错误;
(3)都是由非金属元素形成的化合物可能为离子化合物,如铵盐等,故(3)错误,
故选A.
点评:本题考查元素周期律的作用,难度不大.注意把握元素的递变规律以及对应物质的性质是解题的关键.

练习册系列答案
相关题目
某同学在实验室中进行如表实验:
以下结论正确的是( )
| 编号 | I | Ⅱ | Ⅲ |
| 实验 | 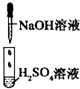 |
 |
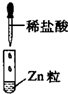 |
| 现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
| A、I中混合前后溶液中各离子种类、个数均不变 |
| B、Ⅱ中反应前后溶液中Cu2+、Cl-浓度均未变 |
| C、Ⅱ中BaCl2替换为Ba(NO3)2溶液,发生的离子反应相同 |
| D、Ⅲ中发生的反应属于置换反应,不属于离子反应 |
在实验室中,下列除去杂质的方法正确的是( )
| A、溴苯中混有溴,加入KI溶液,用汽油萃取 |
| B、乙烷中混有乙烯,通入氢气在一定条件下反应,使乙烯转化为乙烷 |
| C、硝基苯中混有浓硝酸和浓硫酸,将其倒入浓烧碱溶液中,静置,然后分液 |
| D、乙烷中混有乙炔,通入高锰酸钾酸性溶液洗气除去 |
在周期表中存在对角线规则,据此判断下列物质的性质相似性的是( )
| A、氮和硅 | B、铝和铁 |
| C、铍和铝 | D、铜和金 |
下列粒子中核外未成对电子数目最多的是( )
| A、P |
| B、Fe3+ |
| C、Cr |
| D、Cu |
下列物质的变化过程中,没有化学键断裂的是( )
| A、HCl溶解于水 |
| B、NaCl晶体的熔化 |
| C、干冰升华 |
| D、氯化铵的“升华” |
下列各组物质性质的比较中,正确的是( )
| A、热稳定性:NH3<PH3<H2O |
| B、酸性:H3PO4>H2SO4>HClO4 |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、金属性:Na>Mg>Al |
下列关于强弱电解质的叙述正确的是( )
| A、KCl溶液在电流作用下电离成K+和Cl- |
| B、SO2溶于水能部分转化成离子,故SO2属于弱电解质 |
| C、CaSO4微溶于水,所以CaSO4属弱电解质 |
| D、同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不相同 |
下列叙述,正确的是( )
A、人们使用
| ||||
| B、科学家们在过渡元素中寻找催化剂 | ||||
| C、目前周期表中的所有元素都是科学家们从自然界发现的 | ||||
| D、只有主族元素同时由短周期元素和长周期元素共同构成 |