题目内容
常温下,在pH=12的某碱溶液中,由水电离出的c(OH-)为( )
| A、1.0×10-7 mol/L |
| B、1.0×10-6 mol/L |
| C、1.0×10-3 mol/L |
| D、1.0×10-12 mol/L |
考点:弱电解质在水溶液中的电离平衡,水的电离
专题:电离平衡与溶液的pH专题
分析:室温时,Kw=1×10-14,c(H+)×c(OH-)=1×10-14;溶液中碱电离的氢氧根离子抑制了水电离,碱溶液中c(H+)等于水电离出的c(OH-),根据溶液的pH=12,计算出溶液中的氢离子浓度,水电离的氢氧根离子的浓度等于溶液中的氢离子浓度.
解答:
解:室温下,Kw=1×10-14,c(H+)×c(OH-)=1×10-14,在pH=12的某碱溶液中,溶液中的氢离子是水电离的,氢离子浓度为:c(H+)=1×10-12mol/L,所以水电离的氢氧根离子浓度为:1×10-12mol/L,故选D.
点评:本题考查了PH的简单计算和水的电离问题,题目难度不大,注意溶液中PH的计算方法和水的电离特点.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
下列各组物质性质的比较中,正确的是( )
| A、热稳定性:NH3<PH3<H2O |
| B、酸性:H3PO4>H2SO4>HClO4 |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、金属性:Na>Mg>Al |
如图所示的装置中,能够组成原电池,产生电流的是( )
A、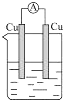 稀硫酸 |
B、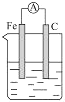 NaCl溶液 |
C、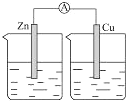 稀盐酸 |
D、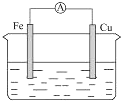 酒精 |
下列叙述,正确的是( )
A、人们使用
| ||||
| B、科学家们在过渡元素中寻找催化剂 | ||||
| C、目前周期表中的所有元素都是科学家们从自然界发现的 | ||||
| D、只有主族元素同时由短周期元素和长周期元素共同构成 |
下列叙述正确的是( )
| A、主族金属元素的化合价均不会超过+4 |
| B、元素周期表中氧元素的位置列出的“16.00”是元素的相对原子质量 |
| C、Na2O2中阳离子与阴离子物质的量之比为1:1 |
| D、含有相同质子数和电子数的两种微粒可能是一种分子和一种离子 |