题目内容
2003年10月16日“神舟五号”飞船成功发射,实现了中华民族的飞天梦想. 运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物.已知该化合物中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键.
(1)该氮氢化合物的电子式为 .
(2)若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,
写出该反应的化学方程式 .
(3)NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl=NH4Cl.
试写出上述氮氢化合物与足量盐酸反应的化学方程式
(4)与该氮氢化合物结构相似的一种有机分子乙二胺H2N-CH2-CH2-NH2简写为en(一对孤对电子可行成一根配位键)该有机物可以和Cu2+形成配合物,试写出该配合离子的化学式 .
(1)该氮氢化合物的电子式为
(2)若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,
写出该反应的化学方程式
(3)NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl=NH4Cl.
试写出上述氮氢化合物与足量盐酸反应的化学方程式
(4)与该氮氢化合物结构相似的一种有机分子乙二胺H2N-CH2-CH2-NH2简写为en(一对孤对电子可行成一根配位键)该有机物可以和Cu2+形成配合物,试写出该配合离子的化学式
考点:氮族元素简介,电子式
专题:氮族元素
分析:(1)该氮氢化合物中N(H)=
=4,故分子中N(N)=
=2,该氮氢化合物为N2H4,分子中氢原子之间形成1对共用电子对,氢原子与氮原子之间形成1对共用电子对;
(2)N2H4与液态双氧水恰好完全反应,产生两种无毒又不污染环境的物质,则生成氮气与水;
(3)N2H4分子中每个N原子都含有1对孤对电子,故1molN2H4与2molHCl反应生成N2H6Cl2;
(4)乙二胺(H2N-CH2-CH2-NH2)有2个氮原子.
| 32×12.5% |
| 1 |
| 32-4 |
| 14 |
(2)N2H4与液态双氧水恰好完全反应,产生两种无毒又不污染环境的物质,则生成氮气与水;
(3)N2H4分子中每个N原子都含有1对孤对电子,故1molN2H4与2molHCl反应生成N2H6Cl2;
(4)乙二胺(H2N-CH2-CH2-NH2)有2个氮原子.
解答:
解:(1)该氮氢化合物中N(H)=
=4,故分子中N(N)=
=2,该氮氢化合物为N2H4,分子中氢原子之间形成1对共用电子对,氢原子与氮原子之间形成1对共用电子对,其电子式为 ,
,
故答案为: ;
;
(2)N2H4与液态双氧水恰好完全反应,产生两种无毒又不污染环境的物质,则生成氮气与水,该反应化学方程式为:N2H4+2H2O2=N2+4H2O,
故答案为:N2H4+2H2O2=N2+4H2O;
(3)N2H4分子中每个N原子都含有1对孤对电子,故1molN2H4与2molHCl反应生成N2H6Cl2,反应方程式为:N2H4+2HCl=N2H6Cl2,
故答案为:N2H4+2HCl=N2H6Cl2;
(4)乙二胺(H2N-CH2-CH2-NH2)有2个氮原子,Cu2+溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+,故答案为:[Cu(En)2]2+.
| 32×12.5% |
| 1 |
| 32-4 |
| 14 |
 ,
,故答案为:
 ;
;(2)N2H4与液态双氧水恰好完全反应,产生两种无毒又不污染环境的物质,则生成氮气与水,该反应化学方程式为:N2H4+2H2O2=N2+4H2O,
故答案为:N2H4+2H2O2=N2+4H2O;
(3)N2H4分子中每个N原子都含有1对孤对电子,故1molN2H4与2molHCl反应生成N2H6Cl2,反应方程式为:N2H4+2HCl=N2H6Cl2,
故答案为:N2H4+2HCl=N2H6Cl2;
(4)乙二胺(H2N-CH2-CH2-NH2)有2个氮原子,Cu2+溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+,故答案为:[Cu(En)2]2+.
点评:本题考查无机物的有关推断、常用化学用语等,难度中等,(3)中注意根据信息理解氨气与HCl反应的本质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在一容积固定的密闭容器中进行反应:2SO2(g)+O2(g)??2SO3(g).已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol?L-1、0.1mol?L-1、0.2mol?L-1.当反应达到平衡时,各物质的浓度可能存在的数据是( )
| A、SO2为0.4 mol?L-1,O2为0.2 mol?L-1 |
| B、SO2为0.25 mol?L-1 |
| C、SO2和SO3均为0.15 mol?L-1 |
| D、SO2为0.4 mol?L-1 |
金属镁溶于很稀的硝酸溶液,生成硝酸镁、硝酸铵和水.反应的镁和HNO3物质的量之比是( )
| A、3:8 | B、1:4 |
| C、2:5 | D、4:1 |
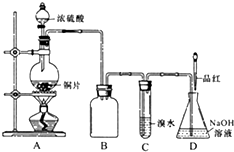 某化学兴趣小组设计实验,用浓硫酸与铜反应制得SO2并进行相关实验探究.
某化学兴趣小组设计实验,用浓硫酸与铜反应制得SO2并进行相关实验探究.