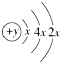题目内容
在一容积固定的密闭容器中进行反应:2SO2(g)+O2(g)??2SO3(g).已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol?L-1、0.1mol?L-1、0.2mol?L-1.当反应达到平衡时,各物质的浓度可能存在的数据是( )
| A、SO2为0.4 mol?L-1,O2为0.2 mol?L-1 |
| B、SO2为0.25 mol?L-1 |
| C、SO2和SO3均为0.15 mol?L-1 |
| D、SO2为0.4 mol?L-1 |
考点:化学平衡的计算
专题:
分析:化学平衡的建立,既可以从正反应开始,也可以从逆反应开始,或者从正逆反应开始,不论从哪个方向开始,物质都不能完全反应,利用极限法假设完全反应,计算出相应物质的浓度变化量,实际变化量小于极限值,据此判断分析.
解答:
解:A、SO2和O2的浓度增大,说明反应向逆反应方向进行建立平衡,若SO3完全反应,则SO2和O2的浓度浓度变化分别为0.2mol/L、0.1mol/L,实际变化应小于该值,故A错误;
B、SO2的浓度增大,说明反应向逆反应方向进行建立平衡,若SO3完全反应,则SO2的浓度浓度变化为0.2mol/L,实际变化为0.05mol/L,小于0.2mol/L,故B正确;
C、反应物、生产物的浓度不可能同时减小,一个减小,另一个一定增大,故C错误;
D、SO3的浓度增大,说明该反应向正反应方向进行建立平衡,若二氧化硫和氧气完全反应,SO3的浓度的浓度变化为0.2mol/L,实际变化小于该值,故D错误.
故选B.
B、SO2的浓度增大,说明反应向逆反应方向进行建立平衡,若SO3完全反应,则SO2的浓度浓度变化为0.2mol/L,实际变化为0.05mol/L,小于0.2mol/L,故B正确;
C、反应物、生产物的浓度不可能同时减小,一个减小,另一个一定增大,故C错误;
D、SO3的浓度增大,说明该反应向正反应方向进行建立平衡,若二氧化硫和氧气完全反应,SO3的浓度的浓度变化为0.2mol/L,实际变化小于该值,故D错误.
故选B.
点评:本题考查了化学平衡的建立,难度不大,关键是利用可逆反应的不完全性,运用极限假设法解答,假设法是解化学习题的常用方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
| A、64g的铜发生氧化还原反应,一定失去2NA个电子 |
| B、任何条件下,4.6g Na和足量的O2完全反应失去电子数都为0.2NA |
| C、常温常压下,氧气和臭氧的混合物16g中约含有6.02×1023个氧原子 |
| D、常温常压下,1mol氦气分子含有的核外电子数为4NA |

 A、B、C、D四种短周期元素,且A、B为同周期元素,B、C同主族,B、C可形成共价化合物BC3和BC2,A、D同主族,A的原子结构示意图为:
A、B、C、D四种短周期元素,且A、B为同周期元素,B、C同主族,B、C可形成共价化合物BC3和BC2,A、D同主族,A的原子结构示意图为: