题目内容
12.新版人民币的发行,引发了人们对有关人民币中化学知识的关注.下列表述不正确的是( )| A. | 制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素 | |
| B. | 用于人民币票面文字等处的油墨中所含有的氧化铁是一种磁性物质 | |
| C. | 防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料 | |
| D. | 某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是淀粉 |
分析 A.棉花、木材的成分为纤维素;
B.氧化铁为红色,四氧化三铁为黑色具有磁性的物质;
C.高分子化合物相对分子质量很大,一般在10000以上,可高达几百万;
D.淀粉遇碘单质变蓝.
解答 解:A.棉花、优质针叶木等原料的主要成分是纤维素,故A正确;
B.Fe3O4是磁性物质,有磁性,则用于人民币票面文字等处的油墨中所含有的四氧化三铁是一种磁性物质,故B错误;
C.树脂相对分子质量很大,属于有机高分子材料,故C正确;
D.淀粉遇碘单质变蓝,则某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,故D正确;
故选B.
点评 本题考查物质的性质与用途,为高频考点,把握物质的性质、化学与生活的关系、发生的反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
3.设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 60g丙醇中存在的共价键总数为11NA | |
| B. | 0.5 mol•L-1 CuCl2溶液中含有的Cl-个数为NA | |
| C. | 标准状况下,H2和CO混合气体8.96L在足量O2中充分燃烧消耗O2分子数为0.2NA | |
| D. | 在反应4Cl2+8NaOH═6NaCl+NaClO+NaClO3+4H2O中,消耗1mol Cl2时转移的电子总数为1.5NA |
20.下图是两种烃的球棍模型,以下说法不正确的是( )
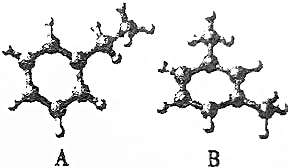

| A. | 二者属于同系物 | B. | 二者都属于芳香烃 | ||
| C. | 二者互为同分异构体 | D. | B可发生加成反应 |
7.化学与科学、技术、社会、环境密切相关,下列有关说法中正确的有( )
| A. | 黑色金属材料通常包括铁、铬、铜以及它们的合金,是应用非常广泛的金属材料 | |
| B. | 烹鱼时加入少量的料酒和食醋可减少腥味,增加香味,属于物理变化 | |
| C. | 若分散质粒子直径在1nm-100nm之间,则其为胶体;放电时放映室射到银幕上的光柱的形成属于丁达尔效应 | |
| D. | Na2CO3•10H2O在干燥空气中失水和木材干馏制焦炭都属于化学变化 |
17.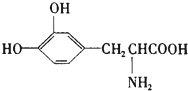 L-多巴胺是一种有机物,它可以用于帕金森综合症的治疗,其结构简式如下
L-多巴胺是一种有机物,它可以用于帕金森综合症的治疗,其结构简式如下
下列关于L-多巴胺的叙述不正确的是( )
 L-多巴胺是一种有机物,它可以用于帕金森综合症的治疗,其结构简式如下
L-多巴胺是一种有机物,它可以用于帕金森综合症的治疗,其结构简式如下下列关于L-多巴胺的叙述不正确的是( )
| A. | 它属于α-氨基酸,既具有酸性,又具有碱性 | |
| B. | 它遇到Fe2(SO4)3溶液显紫色 | |
| C. | 他可以两分子间缩合形成分子式为C18H18O6N2的化合物,该化合物中有3个六元环 | |
| D. | 它既与酸反应又与碱反应,等物质的量的L-多巴胺最多消耗NaOH与HCl物质的量之比为1:1 |
3.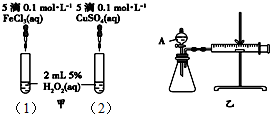 为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.下列叙述中不正确的是( )
为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.下列叙述中不正确的是( )
 为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.下列叙述中不正确的是( )
为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.下列叙述中不正确的是( )| A. | 实验中H2O2分解的速率为(1)>(2) | |
| B. | 图乙实验可通过测定相同状况下,产生的气体体积与反应时间来比较反应速率 | |
| C. | H2O2分解的热化学方程式2H2O2(l)═2H2O(l)+O2(g)△H>0 | |
| D. | 图甲中(1)、(2)两个实验中H2O2分解的△H相同 |
20.(1)某学习小组用相同大小的铝片与3.0mol/L盐酸、1.5mol/L硫酸、3.0mol/L硫酸进行反应速率实验,结果如下:
①反应1~15min内,铝与盐酸的反应速率逐渐加快,其原因是_反应放出热量,温度升高,使化学反应速率加快
②铝无论与1.5mol/L硫酸还是3.0mol/L硫酸进行反应,与盐酸相比都无明显现象,根据以上铝与稀盐酸和稀硫酸反应差异,有人做出了一种假设或者猜想
假设或猜想一:Cl-能促进金属铝与H+的反应
假设或猜想二:SO42-对H+与金属铝的反应起阻碍作用
请将上述猜想补充完整,并验证.除上述试剂外,还有下列试剂可以选择:单质Mg、Na2SO4固体、NaCl固体、硝酸将上述没有明显反应的溶液中加入少量的NaCl固体,如果产生气泡,说明假设一成立
(2)试用简单的一种实验证明,在醋酸溶液中存在着:CH3COOH?H++CH3COO-的电离平衡.限制选试剂和用品:PH试纸、PH=2的醋酸溶液、醋酸钠固体、蒸馏水,仪器任选.写出简要操作、现象.(结论已经给你写好)将pH=2的溶液稀释100后,再测定其pH,若pH小于4,说明醋酸溶液中存在电离平衡说明醋酸溶液中存在电离平衡.
| 反应进程(分钟) | 1 | 2 | 5 | 15 | 20 |
| 3.0mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 1.5mol/L硫酸 | 均无明显现象(无气泡产生) | ||||
| 3.0mol/L硫酸 | 均无明显现象(无气泡产生) | ||||
②铝无论与1.5mol/L硫酸还是3.0mol/L硫酸进行反应,与盐酸相比都无明显现象,根据以上铝与稀盐酸和稀硫酸反应差异,有人做出了一种假设或者猜想
假设或猜想一:Cl-能促进金属铝与H+的反应
假设或猜想二:SO42-对H+与金属铝的反应起阻碍作用
请将上述猜想补充完整,并验证.除上述试剂外,还有下列试剂可以选择:单质Mg、Na2SO4固体、NaCl固体、硝酸将上述没有明显反应的溶液中加入少量的NaCl固体,如果产生气泡,说明假设一成立
(2)试用简单的一种实验证明,在醋酸溶液中存在着:CH3COOH?H++CH3COO-的电离平衡.限制选试剂和用品:PH试纸、PH=2的醋酸溶液、醋酸钠固体、蒸馏水,仪器任选.写出简要操作、现象.(结论已经给你写好)将pH=2的溶液稀释100后,再测定其pH,若pH小于4,说明醋酸溶液中存在电离平衡说明醋酸溶液中存在电离平衡.
1.化学在生产和生活中有重要的应用,下列说法正确的是( )
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子化合物 | |
| B. | 14C可用于文物年代的鉴定,14C与12C互为同素异形体 | |
| C. | 福尔马林可作食品的保鲜剂 | |
| D. | “开发利用新能源”、“汽车尾气催化净化”都能提高空气质量 |
 .
.