题目内容
20.下图是两种烃的球棍模型,以下说法不正确的是( )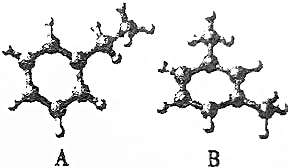
| A. | 二者属于同系物 | B. | 二者都属于芳香烃 | ||
| C. | 二者互为同分异构体 | D. | B可发生加成反应 |
分析 根据原子成键特点知,A为乙苯,B为间二甲苯,
A.两者的分子式相同,不互为同系物;
B.乙苯和间二甲苯均属于芳香烃;
C.乙苯和间二甲苯的分子式相同,结构不同,互为同分异构体;
D.间二甲苯在一定条件下可与氢气发生加成反应.
解答 解:根据原子成键特点知,A为乙苯,B为间二甲苯,
A.两者的分子式相同,不互为同系物,故A选;
B.乙苯和间二甲苯均属于芳香烃,故B不选;
C.乙苯和间二甲苯的分子式相同,结构不同,互为同分异构体,故C不选;
D.间二甲苯在一定条件下可与氢气发生加成反应,故D不选.
故选A.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系、甲烷和乙烯及苯结构特点是解本题关键,侧重考查学生分析判断及知识运用能力.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
11.室温下,甲、乙两烧杯均盛有5mlpH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4,关于甲、乙两烧杯中溶液的描述正确的是( )
| A. | 溶液的体积:V乙≤10V甲 | |
| B. | 若分别与5mlpH=11的NaOH溶液反应,所得溶液的pH:甲≤乙 | |
| C. | 若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 | |
| D. | 水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙 |
15.短周期元素V、X、Y、Z、W原子序数依次增大,其中,V为原子半径最小的原子,X与Y、Z与W的核外电子层数相同,最大层电子数依照Z,X,Y,W的顺序成公差为1的等差数列,元素X、W的原子序数之和是Y的3倍.以下说法中正确的是( )
| A. | 简单离子半径从小到大:V、Y、X、W、Z | |
| B. | X、Y、Z均只能与V形成共价化合物 | |
| C. | 气态氢化物稳定性:X<W,其中的原因是X-V键的键能小于W-V键 | |
| D. | Z与碳元素形成的一种常见化合物的分子式为ZC |
5.下列说法正确的是( )
| A. | 2012年,随着两会顺利召开,保障房建设成为热点.住宅建设离不开硅酸盐材料,工业玻璃、水泥、陶瓷都要使用石灰石做原料,钢筋混凝土、玻璃钢、石棉瓦、碳纤维增强陶瓷都是常见的复合材料 | |
| B. | 去年底,世界气候大会在南非德班召开.开发新型能源是践行低碳生活的有效途径之一,生物质能是指来源于动植物及其加工产品所储存的能量 | |
| C. | 近年食品安全倍受关注,某媒体披露“皮革奶”事件.有不法厂商将皮革下脚料水解后掺入奶粉以提高奶粉中蛋白质的含量.动物皮革的主要成分是蛋白质,“皮革奶”灼烧时有烧焦羽毛的气味 | |
| D. | 氯化钙及氯化镁等“化冰盐”是冰融化成水的反应催化剂,在雪地里加入化冰盐可快速消除冰雪 |
12.新版人民币的发行,引发了人们对有关人民币中化学知识的关注.下列表述不正确的是( )
| A. | 制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素 | |
| B. | 用于人民币票面文字等处的油墨中所含有的氧化铁是一种磁性物质 | |
| C. | 防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料 | |
| D. | 某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是淀粉 |
8.某小组研究影响反应速率的因素..
(1)实验一:探究酸的强弱对酸与镁条反应速率的影响.
①设计实验方案如下表,表中c=1.0 mol•L-1.
②实验步骤:a)检查装置(图1)的气密性后,添加药品;
b)反应开始后,每隔1min记录一次生成H2的体积;
c)将所记录的数据转化为曲线图(图2).
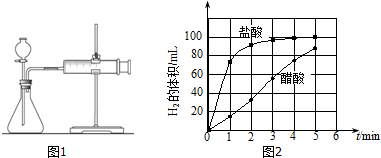
③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律:醋酸与镁条反应的速率随时间变化不明显,盐酸与镁条反应开始阶段反应速率很快,一段时间后反应速率明显减小.
(2)实验二:探究反应条件对0.10mol/L Na2S2O3溶液与稀H2SO4反应速率的影响.其设计与测定结果如下:
①完成上述反应原理的离子反应方程式S2O32-+2H+═S↓+H2O+SO2↑
②上述实验①③是探究温度对化学反应速率的影响;若上述实验①②是探究浓度对化学反应速率的影响,则表格中“甲”应填写V(蒸馏水)/mL,a为5.0;乙是实验需要测量的物理量,则表格中“乙”应填写出现浑浊的时间/min.
(1)实验一:探究酸的强弱对酸与镁条反应速率的影响.
①设计实验方案如下表,表中c=1.0 mol•L-1.
| 编号 | 酸的种类 | 酸的浓度/mol•L-1 | 酸的体积/mL | 镁条质量/g |
| 1 | 醋酸 | 1.0 | 10 | 2.0 |
| 2 | 盐酸 | c | 10 | 2.0 |
b)反应开始后,每隔1min记录一次生成H2的体积;
c)将所记录的数据转化为曲线图(图2).

③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律:醋酸与镁条反应的速率随时间变化不明显,盐酸与镁条反应开始阶段反应速率很快,一段时间后反应速率明显减小.
(2)实验二:探究反应条件对0.10mol/L Na2S2O3溶液与稀H2SO4反应速率的影响.其设计与测定结果如下:
| 编号 | 反应温度/℃ | Na2S2O3溶液/mL | 甲 | 0.10mol/L H2SO4溶液/mL | 乙 |
| 1 | 25℃ | 10.0 | 0 | 10.0 | |
| 2 | 25℃ | 5.0 | a | 10.0 | |
| 3 | 45℃ | 10.0 | 0 | 10.0 |
②上述实验①③是探究温度对化学反应速率的影响;若上述实验①②是探究浓度对化学反应速率的影响,则表格中“甲”应填写V(蒸馏水)/mL,a为5.0;乙是实验需要测量的物理量,则表格中“乙”应填写出现浑浊的时间/min.
9.在多电子原子中,轨道能量是由以下哪些因素决定( )
①能层 ②能级 ③空间伸展方向 ④自旋状态.
①能层 ②能级 ③空间伸展方向 ④自旋状态.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |